
时间:2022-09-27 12:01:51来源:网络整理
瑞仪(高中)化学专业和有“铍”气的同学都在关注!
实验一:
蒸馏实验:
蒸馏:利用相互液体混合物中各组分的不同沸点(一般相差30℃以上)进行分离提纯的方法。
实验室蒸馏石油
1. 为什么油叫混合物?蒸馏的各种馏分是纯的还是混合物?
石油中含有多种烷烃和环烷烃,所以是混合物。各种馏出物
馏分也是混合物,因为蒸馏是一种物理变化。
2. 在原油中添加几块碎陶瓷或碎玻璃是如何工作的?防撞。
3. 温度计水银球的位置和作用是什么?将其插入蒸馏瓶支管口的稍下部氨水浓度检测,以测量蒸汽的温度。
4. 一个蒸馏装置由多少部分组成?零件的名称是什么?中间冷凝机组冷却水的流向是什么?
四部分:蒸馏瓶、冷凝管、接收器、锥形瓶。冷却水从下端进水口进入,从上端出水口流出。
5. 收集的直馏汽油会使酸性 KMnO4 溶液变色吗?溴水会褪色吗?为什么?
酸性KMnO4溶液不会变色,但溴水会因萃取而变色,因为蒸馏是一种物理变化,蒸馏出来的各个馏分仍然是由各种烷烃和环烷烃组成。
实验2:萃取:利用物质在不混溶溶剂中的溶解度差异,将物质从一种溶剂转移到另一种溶剂中分离物质的方法。常用的萃取剂有苯、乙醚、二氯甲烷、CCl4等。
【萃取剂的选择】①萃取剂与原溶剂互不混溶,不发生反应②溶质在萃取剂中的溶解度远大于在原溶剂中的溶解度③溶质不与萃取剂反应
▲分离:常用于两种不混溶液体的分离纯化。
实验 3:煤的干馏
1. 为什么要挡风?蒸煮是物理变化还是化学变化?煤的干馏和木材的干馏可以得到哪些物质?
在空气中有氧气的情况下,煤会燃烧。干馏是一种化学变化,煤的干馏可以得到焦炭、焦炉煤气、煤焦油、粗氨;木材干馏可得到木气、木炭、木焦油
2. 点燃收集到的气体,会发生什么?在直试管中取少量冷凝液,滴入紫色石蕊试液中。这是什么现象,为什么?
气体安静地燃烧,产生淡蓝色的火焰。它能使石蕊试液变蓝,因为这种液体是粗氨水,溶于氨水,在水中电离成碱性。
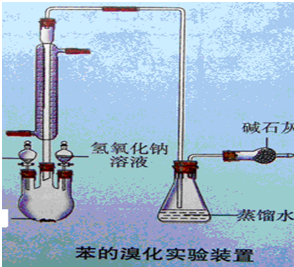
实验4:制备溴苯和硝基苯的实验:
一、溴苯的制备:
1. 反应方程式:
2. 长导管在设备中的作用是什么?空气传导和冷凝。溴和苯的缩合反应(回流原理)
3. 添加的铁粉是如何工作的?催化剂(严格来说,真正起催化作用的是FeBr3)
4. 导管末端的白雾是什么成分?原因?如何吸收和测试?在锥形瓶中,为什么导管不能延伸到液面以下?
白雾是一小滴氢溴酸,因为 HBr 极易溶于水而形成。用水吸收。测试酸化的AgNO3溶液:用硝酸加入酸化的AgNO3溶液后,产生淡黄色沉淀。导管端口不突出低于液面,以防止水被吸回。
5. 将反应后的液体倒入装满冷水的烧杯中氨水浓度检测,会发生什么?
水面下棕色油状液体(溴苯比水重,不溶于水)
6. 如何清洗产品以恢复其原有颜色?
溴苯因溶解溴而呈棕色。可用水、稀NaOH溶液和水洗涤纯化。
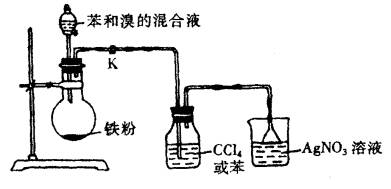
7、探索:如何验证反应是取代反应?验证产品 HBr
在原装置中,在烧瓶和锥形瓶之间加入装有苯或CCl4的试管除去Br2,将硝酸酸化的AgNO3溶液滴加到锥形瓶中的水溶液中,产生淡黄色沉淀或量取锥形瓶中的水溶液。酸碱度,酸碱度
二、硝基苯制备实验方案及实验步骤
①混合酸的制备:先将1.5 mL浓硝酸倒入大试管中,再缓慢倒入2 mL浓硫酸,摇匀,及时冷却。(注意添加酸的顺序)
② 向冷却后的混合酸中滴加苯 1 mL,摇匀,混匀。【来源:主题网ZXXK】
③将大试管在50-60℃水浴中加热10分钟左右。实验装置如图 2-5 所示。
④ 将反应后的液体倒入装有冷水的烧杯中。可以观察到在烧杯底部形成黄色油状物质。使用分液漏斗分离粗硝基苯。
⑤粗品依次用蒸馏水和5%NaOH溶液洗涤,最后用蒸馏水洗涤。如果将用无水氯化钙干燥的粗硝基苯进行蒸馏,即可得到纯硝基苯。蒸馏应在通风橱或通风良好的地方进行。
纯硝基苯是一种无色油状液体,具有比水更浓的苦杏仁味。
1. 反应方程式:
2.要将浓HNO3和浓H2SO4的混合酸冷却到50-60℃以下,为什么?
①防止浓HNO3分解 ②防止热混合使苯和浓HNO3挥发
③温度过高会发生副反应(生成苯磺酸和间二硝基苯)
3. 将一根导管插入装有反应液的大试管上端有什么作用?冷凝回流(苯和浓硝酸)
4. 温度计水银球的位置和作用是什么?插入水浴中以测量水浴的温度。
5. 为什么要用水浴加热?在 60°C 左右的水浴中加热 10 分钟的目的是什么?为什么要控制温度,不能太高?
水浴加热,温度控制方便。有机反应往往很慢,加热 10 分钟可使反应完成。①防止浓NHO3分解 ②防止热混合使苯和浓HNO3挥发 ③温度过高会发生副反应(生成苯磺酸)
酸和间二硝基苯)
6. 制成品的颜色、密度、水溶性、气味如何?怎么洗才能恢复原来的颜色?
淡黄色(溶于NO2,颜色应为无色),油状液体,密度高于水,不溶于水,有苦杏仁味。它通过用水、NaOH溶液和水洗涤来纯化。
水浴加热,温度控制方便。有机反应往往很慢,加热 10 分钟可使反应完成。①防止浓NHO3分解 ②防止热混合使苯和浓HNO3挥发 ③温度过高会发生副反应(生成苯磺酸和间二硝基苯)
6. 制成品的颜色、密度、水溶性、气味如何?怎么洗才能恢复原来的颜色?
淡黄色(溶于NO2,颜色应为无色),油状液体,密度高于水,不溶于水,有苦杏仁味。它通过用水、NaOH溶液和水洗涤来纯化。
实验5:苯和苯同系物的区别:(测试)
实验:将苯、甲苯和二甲苯2mL分别注入3支试管中,每支加入3滴KMnO4酸溶液,剧烈摇晃溶液,观察溶液颜色变化。
现象:
综上所述:
实验6:溴乙烷取代反应、消除反应
一、取代反应
(1) 原料:溴乙烷、NaOH水溶液
(2)反应原理:CH3CH2Br + NaOH
CH3CH2OH + 溴化钠
(3)卤代烃中卤素的验证
①将少量卤代烃放入试管中,加入NaOH溶液;②将试管中的混合物加热至沸腾;③冷却,加稀硝酸酸化;④加入硝酸银溶液,观察沉淀的颜色。
实验说明:
①溴乙烷在水中不能电离Br-,它是一种非电解质,加入AgNO3溶液不会产生淡黄色沉淀。②加热煮沸的目的是为了加快卤代烃的水解反应速度,因为不同的卤代烃水解的难易程度不同。
③加硝酸酸化,一是中和过量的NaOH,防止NaOH与硝酸银反应形成棕色Ag2O沉淀干扰实验现象;二是检查生成的沉淀是否溶于稀硝酸。【来源:主题网ZXXK】
同理,还有淀粉水解液的测试:淀粉水解是在酸性条件下进行的,而葡萄糖的醛基是在碱性条件下测试的,所以在加入银氨溶液或新制备的氢氧化铜之前必须先加氢。钠溶液中和过量的酸。
二、消除反应:原料:溴乙烷、NaOH酒精溶液
在溴乙烷和氢氧化钠的乙醇中
在消除反应过程中观察到气体(乙烯)的形成。用高锰酸钾溶液检测乙烯气体前,必须
除去装满水的试管中可能含有的任何乙醇,因为乙醇可被高锰酸钾氧化使溶液变色,或直接通溴水。
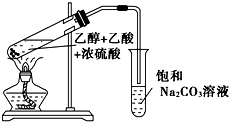
实验7:乙醇的性质----消除反应:乙烯的制备和性质
1. 化学方程式:
2. 哪个工厂用于生产乙烯?该装置还能产生哪些其他气体?
一套分液漏斗和圆底烧瓶(加热)装置;该装置还可生产Cl2、HCl、SO2等。
3. 提前往烧瓶里加几片碎玻璃(碎片)的目的是什么?
防止颠簸(防止混合物受热时剧烈弹跳)
4. 乙醇与浓硫酸混合,有时得不到乙烯。可能是什么原因?
这主要是因为温度没有迅速升高到170℃,因为在140℃乙醇会发生分子间脱水得到乙醚,方程式:
5. 水银球在温度计上的位置和作用是什么?在混合液液位以下,用于测量混合液的温度(控制温度)。
6.浓H2SO4的作用?催化剂、脱水剂。
7、20mL 1:3乙醇和浓硫酸混合液的制备方法:在烧杯中加入5mL 95%乙醇,再滴加15mL浓硫酸,边加边搅拌,冷却备用。注意不能反向逐滴添加,否则由于
混合放热可能导致液体飞溅伤人。
8、反应后期,有时反应液会变黑,并产生有刺鼻气味的气体,为什么?检测乙烯气体需要注意什么?
浓硫酸碳化氧化乙醇,产生刺激性气味气体为SO2,
检测乙烯气体前,应先用氢氧化钠溶液除去CO2、SO2、冷凝的乙醇蒸气(如图)。
实验 8:苯酚的性质
一、溶解度、酸度等实验:
现象:苯酚水溶液浑浊→加入氢氧化钠溶液后变清→加入稀盐酸或通入CO2后变浑浊
解释:苯酚在常温下在水中溶解度低→苯酚与氢氧化钠溶液反应生成苯酚钠,易溶于水→强酸生成弱酸,苯酚不溶于水
二、酚醛树脂
取代反应:实验重点:苯酚稀溶液、饱和溴水。在浓苯酚溶液和稀溴水的情况下,不会出现沉淀,因为三溴苯酚会溶解在苯酚溶液中。
三、颜色反应:苯酚和所有苯酚在 FeCl3 溶液中变成紫色。无色的酚晶体可被空气中的氧气氧化成粉红色,其他酚类也可被氧化,使酸性高锰酸钾溶液褪色。
实验 9:乙醛的性质
一、乙醛与银氨溶液反应
(1)反应原料:2%AgNO3溶液、2%稀氨水、乙醛稀溶液【来源:科学.科.网ZXX K】
(2)反应原理:CH3CHO + 2Ag (NH3)2OH
CH3COONH4 + 2Ag ↓+ 3NH3 +H2O
(3)反应装置:试管、烧杯、酒精灯、滴管
银氨溶液的制备:取一个干净的试管,加入1 mL 2%的硝酸银,摇匀,同时滴加2%的稀氨水,直至沉淀溶解。(注:顺序不可颠倒)
(4)注:
①制备银氨溶液时加入的氨水量要适当,不能超过
必须立即准备和使用,不能长时间放置,否则会产生容易爆炸的物质。
②实验中使用的试管必须干净,尤其是无油渍。
③必须用水浴加热,不能直接放在火焰上(否则会产生爆炸性物质),水浴温度不宜过高。
④如果试管不干净,或加热时振动,或加入过量乙醛,则不会形成明亮的银镜,而只会形成黑色的松散沉淀物,或者虽然银可以粘附在试管内壁上,颜色为黑色。
⑤ 实验完成后,应及时处理试管内的混合液,并及时用少量硝酸溶解试管壁上的银镜,然后用水冲洗干净。(废液不可乱倒,应倒入废液罐)
成败关键: 1、试管要干净。2.温水浴加热 3. 4.不能搅拌。溶液呈碱性。5.银氨溶液只能临时配制
,不能长时间放置,氨水的浓度应为2%。.
能产生银镜的物质:1.甲醛、乙醛、乙二醛等各种醛类2.甲酸及其盐类,如HCOOH、HCOONa等3.甲酸盐,如甲酸乙酯 HCOOC2H5、甲酸丙酯 HCOOC3H7 等
4.分子中含有醛基的糖类,如葡萄糖和麦芽糖
清洁方法
实验前用热的氢氧化钠溶液冲洗试管,然后用蒸馏水冲洗
实验结束后,可用硝酸清洗试管中的银镜。硝酸能氧化银生成硝酸银、一氧化氮和水。
银镜反应的应用:常用于醛基的定量和定性检测;也可用于制作瓶胆和镜子。
二、乙醛被新制备的 Cu(OH)2 氧化
(1)反应原料:10%NaOH溶液、2%CuSO4溶液、乙醛稀溶液
(2)反应原理:CH3CHO + 2Cu(OH)2+NaOH
CH3COONa + Cu2O↓+ 3H2O
(3)反应装置:试管、酒精灯、滴管
(4)注:
① 本实验必须在碱性条件下成功。
②Cu(OH)2悬浮液必须立即配制使用,CuSO4溶液的质量分数不宜过大,NaOH溶液宜过量。如果CuSO4溶液过量,在实验过程中不会得到砖红色的Cu2O沉淀(但会得到黑色的CuO沉淀)。
在制备新的 Cu(OH)2 时,试剂按顺序逐滴加入 NaOH - 几滴 CuSO4 - 醛。相对于试剂过量的 NaOH
反应条件:溶液应为
声明:文章仅代表原作者观点,不代表本站立场;如有侵权、违规,可直接反馈本站,我们将会作修改或删除处理。
图文推荐

2022-09-27 11:40:14

2022-09-27 10:57:02

2022-09-27 10:14:15

2022-09-27 09:31:12

2022-09-27 08:48:10

2022-09-26 20:16:02
热点排行
精彩文章

2022-09-27 12:01:37

2022-09-27 11:40:28

2022-09-27 11:40:17

2022-09-27 10:57:05

2022-09-27 10:14:29

2022-09-27 10:02:33
热门推荐
