
时间:2022-07-08 13:01:54来源:网络整理
物质结构知识的一般规则和特殊情况
一、原子结构和元素属性
1. 稀有气体元素原子的最外层一般是具有8个电子的稳定结构。但是He的最外层是一个有2个电子的稳定结构。
2. 原子一般由质子、中子和核外电子组成。但是
它只由质子和电子组成。
3. 金属元素原子的最外层电子数一般小于4,而非金属元素原子的最外层电子数一般大于或等于4。 H、He、B的最外层电子数均小于4,其中H、B为非金属元素,He为稀有气体元素;虽然Ge、Sn、Pb、Bi的最外层电子数都大于等于4,但它们都是金属元素。
4. 仅包含非金属元素的离子通常是阴离子。但也有一些阳离子,比如
等等
5. 非金属元素通常形成阴离子。但是,氧元素形成的离子除了
,和
.
6. 主族元素原子得失电子形成的阴阳离子最外层,一般具有8个电子的稳定结构。但是对于核外只有一个电子壳的离子,最外层只有两个电子,如
;而
它是一个氢核。
7. 含金属离子通常是阳离子。但也有一些阴离子,比如
等等
8. 主族元素的最高价数一般等于原子最外层的电子数。然而,氟和氧的最高价不等于原子最外层的电子数。氟的最高价为0(氟没有正价)硅酸镁溶解度,而氧的最高价为+2(在OF2中)。
9. 化合物中的氢通常为+1。但在金属氢化物中是-1价。
10. 化合物中的氧通常为-2。但在过氧化物中(例如
等),它是-1 价; OF2为+2价。
11. 元素的金属丰度顺序与金属活性的顺序大体一致。但Sn和Pb的金属丰度:Sn
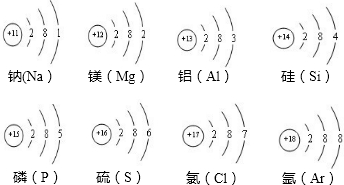
12.对于相应的阴离子和阳离子具有相同电子层结构的金属元素和非金属元素,金属元素的最高价数一般低于非金属元素。和
和
虽然电子层结构是一样的。但钠、镁、铝的最高价(分别为+1、+2、+3价)高于氟的最高价(0价)。
13. 一个原子的相对原子质量通常是保留的有效位数的一小部分。但是12C的相对原子质量是整数和精确值。
14. 随着元素原子序数的增加,元素的相对原子质量一般会依次增加。但18号元素氩的相对原子质量大于19号钾。
15.非金属元素的氢化物在常温下一般为气态,故称气态氢化物,但氧的氢化物H2O为液态。
16. 一个原子的相对原子质量一般不等于对应元素的相对原子质量。但是对于一些只有一种核素的元素,原子的相对原子质量就是该元素的相对原子质量。例如,钠只有一种核素。因此,Na原子的相对原子质量就是钠元素的相对原子质量。原子质量。
二、分子结构
1. 原子间形成的共享电子对一般是由结合在一起的原子提供电子来提供的。但是在
然而,每个都有一个共享的电子对,由N原子和O原子单方面提供,并通过与一个氢原子共享形成。
2. 在物质分子中,每个原子的最外层一般都达到一个稳定的结构,有8个电子。但也有一些物质例外硅酸镁溶解度,如:在气态氢化物中,最外层的氢原子实现了2个电子的稳定结构;在PCl5中,P原子的最外层有10个电子。
3. 化学键一般存在于物质中。但是惰性气体中没有化学键,只有分子间作用力。
4. 大多数气体由双原子分子组成。但是惰性气体是由单原子分子组成的,而臭氧是由三原子分子组成的。
5. 由非金属元素组成的化合物一般是共价化合物。但也有一些是离子化合物,如NH4NO3等铵盐。
6. 由金属元素和非金属元素组成的化合物一般是离子化合物,但也有一些是共价化合物,如:含金属元素的酸分子(如HMnO4、HAlO2)、AlCl3 等
7. 阴离子和阳离子通常形成离子化合物。然而,一些阴离子和阳离子相互作用形成分子或新离子,例如:
.
8.极性分子必须含有极性键,也可能含有非极性键,如:H—O—O—H等
9. 非极性分子不一定只有非极性键,有的只含有极性键,有的同时含有极性和非极性键。如CH4、CH
CH 等人。
10. 离子化合物中通常不存在分子,但离子分子确实以气态存在。如:气态NaCl以a存在
还有一个
由 NaCl 分子组成。
11. 离子化合物必须含有离子键,也可能含有极性或非极性共价键,如:NH4Cl、Na2O2等。
12.元素分子一般是非极性分子,而O3是极性分子。
高考科学与综合化学易出错知识点:“化学实验”部分
1.银氨溶液、氢氧化铜悬浮液、氢硫酸等试剂不宜长期存放,应立即配制使用
正确,银氨溶液易生成Ag3N,极易爆炸
2.实验室制氧后,先取出气瓶,再取出导管,再停止加热
正确
3.品红色试纸、醋酸铅试纸、pH试纸、石蕊试纸使用前必须用蒸馏水润湿
错误,PH试纸不湿
4. 用标准盐酸滴定未知 NaOH 溶液时,所用锥形瓶不能用未知 NaOH 溶液冲洗
正确
5.为防止挥发,浓氨、氢氟酸、漂白粉、液溴、汽油、乙酸乙酯等必须密封保存
错误,漂白粉不易挥发,易腐烂,需要密封保存
6.浓H2SO4沾到皮肤上,立即用水冲洗干净,然后用干布擦拭,最后涂上NaHCO3溶液
错了,先用干布擦拭,再用水冲洗,最后涂上碳酸氢钠溶液
7.在25mL的滴定管中,液位刻度为12.00,则其中所含液体的体积大于13.00mL
正确
8.准确量取25.00mL KMnO4溶液,使用50mL碱性滴定管
错误,使用酸滴定管
9.分离时,分液漏斗下层液体从下口排出,上层液体从上口倒出
正确
10. 蒸馏时,温度计的水银球应放在靠近蒸馏瓶支管口的地方。在下面的实验温度计上分析水银球的位置。 (溶解度测定、乙烯、硝基苯、苯磺酸、酚醛树脂的制备、乙酸乙酯的制备及水解、糖的水解)溶解度的测定(试管水)、乙烯的制备(反应液)、硝基苯(水浴) 、苯磺酸(水浴)、酚醛树脂(沸水浴)、乙酸乙酯制备(直接加热)、水解(水浴)、糖水解(水浴)
11.滴定时,左手控制滴定管的活塞,右手握住锥形瓶,边滴边摇动,观察滴定管内液位下降的速度用眼睛
错误,锥形瓶中的指示器颜色改变了
12.称量时,称量物体放在称量纸上,放在天平右盘,砝码放在天平左盘
错误,左对象右代码
13. 将无色溶液倒入试管中密封,加热试管,溶液变红,冷却后变无色。确定溶液的组成
应该是SO2+品红色溶液
14.甲苯、氯仿、己烯、酒精、苯酚水溶液、纯碱溶液只需一种试剂即可鉴别
正确的浓缩溴水
15. 用氢氧化钠溶液滴定醋酸时,通常选用甲基橙作为指示剂,终点颜色由橙色变为黄色
错了,一般选择酚酞做指示剂
16.盐析法去除蛋白质溶液中的可溶性盐
错误,应该使用透析
17.制备硫酸亚铁溶液所用的蒸馏水应提前煮沸,以除去水中溶解的氧气
正确
18.试管、蒸发皿、坩埚、锥形瓶等仪器可以直接在酒精灯的火焰上加热
不对,锥形瓶应该通过石棉网稍微加热
19. 所谓硅胶就是硅酸胶体。硅胶变色是物理变化误差,硅胶是nSiO2mH2O
硅胶变色是一种化学变化,颜色因CoCl2的水合分子量不同而不同
[CoCl2H2O(蓝色)CoCl26H2O(红色)]
20. 饱和纯碱溶液可以去除乙酸乙酯中的乙酸;油皂化渗析分离得到的混合物
错误,应该加盐
声明:文章仅代表原作者观点,不代表本站立场;如有侵权、违规,可直接反馈本站,我们将会作修改或删除处理。
图文推荐

2022-07-08 10:02:06

2022-07-07 17:01:55

2022-07-07 16:01:52

2022-07-07 15:11:29

2022-07-07 15:01:08

2022-07-07 12:01:28
热点排行
精彩文章

2022-07-08 11:02:50

2022-07-08 09:01:36

2022-07-07 18:00:39

2022-07-06 16:04:34

2022-07-05 12:01:25

2022-07-03 15:03:01
热门推荐
