
时间:2022-02-27 11:58:10来源:
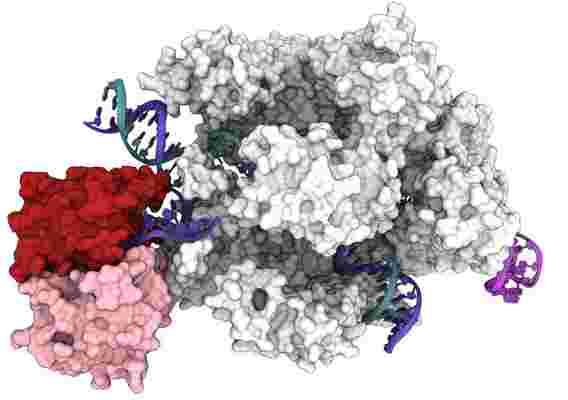
基本编辑器的3D结构,由Cas9蛋白(白色和灰色)和脱氨酶蛋白(红色和粉红色)组成,该Cas9蛋白与互补于RNA向导(紫色)的DNA靶标(蓝绿色和蓝色螺旋)结合,将一个核苷酸换成另一个。
在短短八年内,CRISPR-Cas9成为基础研究和基因治疗的首选基因组编辑器。但是CRISPR-Cas9还产生了其他潜在强大的DNA操作工具,可以帮助修复导致遗传性疾病的基因突变。
加利福尼亚大学伯克利分校的研究人员现在已经获得了这些工具中最有前途的工具的第一个3D结构:与DNA结合并且不需切割即可精确地将一个核苷酸替换为另一个的碱基编辑器。
最初创建于4年前的碱基编辑器已用于尝试纠正人类基因组中的单核苷酸突变。现在可用的基本编辑器可以解决仅由一个核苷酸突变引起的所有已知遗传疾病中大约60%的问题(可能超过15,000种遗传性疾病)。
详细的3D结构发表在7月31日的《科学》杂志上,为调整基础编辑器提供了一个路线图,以使基础编辑器更加通用和可控,可用于患者。
加州大学伯克利分校的博士后研究员加文·诺特(Gavin Knott)说:“我们能够首次观察到一位基本的编辑在行动。”“现在,我们不仅可以了解何时可以使用,什么时候不可以使用,还可以设计下一代基础编辑器,使它们变得更好,更适合临床。”
基本编辑器是一种Cas9融合蛋白,它使用了部分失活的Cas9-剪断剪被禁用,因此只能剪切一条DNA链-一种酶,例如,可以激活或沉默基因,或修饰相邻区域DNA。由于这项新研究报告了Cas9融合蛋白的第一个结构,因此可以帮助指导无数其他基于Cas9的基因编辑工具的发明。
“实际上,我们第一次看到基本编辑器表现为两个独立的模块:您可以使用Cas9模块来提供特异性,然后使用催化模块来提供活性。”前加州大学伯克利分校的博士后研究员Audrone Lapinaite说,他现在是坦佩的亚利桑那州立大学的助理教授。“从这个基础编辑器得到的与目标结合的结构,实际上为我们提供了一种思考Cas9融合蛋白的方式,使我们知道了Cas9的哪个区域更适合融合其他蛋白。”
Lapinaite和Knott最近是澳大利亚莫纳什大学(Monash University)的研究员,并且是该论文的第一作者。
加州大学伯克利分校分子与细胞生物学和化学教授,霍华德·休斯医学研究所研究员,资深作家詹妮弗·道德纳说:“这种结构有助于我们更深入地了解基础编辑。”“现在我们可以看到我们正在使用的工具,我们可以制定明智的策略来改进系统。”
2012年,研究人员首先展示了如何重新构建细菌酶Cas9,并将其转变为从细菌到人类的所有类型细胞的基因编辑工具。CRISPR-Cas9是Doudna和她的法国同事Emmanuelle Charpentier的创意,已经改变了生物学研究并将基因疗法带入临床数十年来。

基本编辑器的3D结构可编辑一段DNA。
科学家们很快选择了Cas9来生产一系列其他工具。基本上,Cas9是蛋白质和RNA的混合物,它精确地靶向特定的DNA片段,然后像一把剪刀一样精确地将其剪断。剪刀的功能可以被破坏,但是,允许Cas9靶向并结合DNA而无需切割。这样,Cas9可以将不同的酶运送到DNA的目标区域,从而允许这些酶操纵基因。
2016年,哈佛大学的David Liu和麻省理工学院和哈佛大学广泛研究所将Cas9与另一种细菌蛋白结合在一起,以外科方式精确地将一个核苷酸替换为另一个核苷酸:第一位基础编辑。
早期的腺嘌呤基础编辑器运行缓慢,而最新版本的ABE8e却快得令人眼花:乱:它在15分钟内完成了将近100%的预期基础编辑。但是,ABE8e可能更倾向于在试管中编辑意外的DNA片段,从而潜在地产生所谓的脱靶效应。
新发现的结构是通过称为低温电子显微镜(cryoEM)的高能成像技术获得的。活性分析表明了为什么ABE8e容易产生更多脱靶编辑:与Cas9融合的脱氨酶蛋白始终处于活跃状态。当Cas9在细胞核周围跳跃时,它会结合并释放成百上千的DNA片段,然后才能找到其预期的靶标。所附的脱氨酶就像是一门松散的大炮,不会等待完美的匹配,而是经常在Cas9停在其最终目标之前对其进行编辑。
知道效应子结构域和Cas9是如何连接的可以导致重新设计,使酶仅在Cas9找到其靶标后才具有活性。
“如果您真的想设计真正特异性的融合蛋白,则必须找到一种使催化结构域更多地成为Cas9一部分的方法,以便它可以感知Cas9何时位于正确的靶标上,然后才被激活,而不是被激活Lapinaite说:“一直都很活跃。”
ABE8e的结构还指出了脱氨酶蛋白的两个特定变化,使其比基础编辑器的早期版本ABE7.10更快地工作。这两个点突变使蛋白质能够更紧紧地抓住DNA,并更有效地将G替换为A。
“作为结构生物学家,我真的很想研究一个分子,并思考合理改进它的方法。这种结构和伴随的生物化学确实为我们提供了这种力量。”诺特补充说。“我们现在可以为该系统在细胞中的行为做出合理的预测,因为我们可以看到它并预测它将如何破裂或预测使其变得更好的方式。”
“获得基础博士学位的人现在被广泛用于介绍从细菌到植物再到灵长类动物等生物的精确变化,但以前没有人观察到基础编辑器的三维分子结构。”于1999年从加州大学伯克利分校获得,现为霍华德·休斯医学研究所的研究员。“这个合作项目揭示了最新的,高度活跃的碱基编辑器ABE8e的美丽分子结构,该分子陷入了与目标DNA位置的交涉。”
参考:Audrone Lapinaite,Gavin J. Knott,Cody M. Palumbo,Enrique Lin-Shiao,Michelle F. Richter,Kevin T. Zhao,Peter A. Beal,David R Liu和Jennifer A.Doudna,2020年7月31日,《科学》。
10.1126 / science.abb1390
除了Lapinaite,Knott,Doudna和Liu之外,其他论文的合著者还包括加州大学戴维斯分校的Cody Palumbo和Peter Beal,加州大学伯克利分校的恩里克·林·肖奥和博德学院的Michelle Richter和Kevin Zhao,这是哈佛大学与哈佛大学之间的合作麻省理工学院。
声明:文章仅代表原作者观点,不代表本站立场;如有侵权、违规,可直接反馈本站,我们将会作修改或删除处理。
图文推荐

2022-02-27 09:58:03

2022-02-27 08:58:03
2022-02-26 19:58:03

2022-02-26 17:58:03

2022-02-26 16:58:03

2022-02-26 08:58:03
热点排行
精彩文章

2022-02-27 11:58:08

2022-02-27 08:58:04

2022-02-26 19:58:06

2022-02-26 18:58:04

2022-02-26 14:58:04

2022-02-26 11:58:04
热门推荐
