
时间:2022-09-11 14:02:16来源:网络整理
高中化学第一章是开辟本学期学习重点的重要途径原子结构与元素性质,必修二仍强调这一点。以下是小编为大家带来的高中化学必修二章第一章的知识点。不要凭直觉低估考试中单个章节的重要性。高中化学必修2第1章知识点(一)1、原子半径
(1)除第一周期外,其他周期元素(惰性气体元素除外)的原子半径随着原子序数的增加而减小;
(2)同族元素从上到下,原子半径随着电子层数的增加而增加。
2、元素价
(1)除第一个循环外,同一循环从左到右,元素最高正价从碱金属+1增加到+7,非金属元素负价增加从碳基-4到-1(氟无正价,氧无+6价除外);
(2)同一主族元素最高正负价数相同
(3)所有元素均显示零价格
3、元素的熔点
(1)随着同周期元素原子序数的增加,单质金属元素的熔点升高,非金属元素的熔点降低;
(2)同组元素从上到下,单质金属元素熔点降低,非金属元素熔点升高
4、元素的金属性和非金属性(及其判断)
(1)同一周期元素的电子壳层数相同。因此,随着核电荷数的增加,原子获得电子的可能性更大。从左到右,金属丰度减少,非金属性增加;
(2)同一主族元素的最外层电子数相同,所以电子层数越多,原子失去电子的可能性越大,金属丰度从自上而下,非金属性降低。
p>
判断金属的强度
金属(还原性)1、越容易从水或酸中置换出氢,越强
2、最高价氧化物的水合物碱性更强(1-20号,K最强;整体Cs最强
非金属(氧化性)1、越容易与氢气反应生成气态氢化物
2、氢化物越稳定
3、最高价氧化物水合物的酸性越强(1-20号,F最强;大多数体相同)
5、原子结构:如:质子数与质量数、中子数、电子数的关系
6、元素周期表和元素周期律
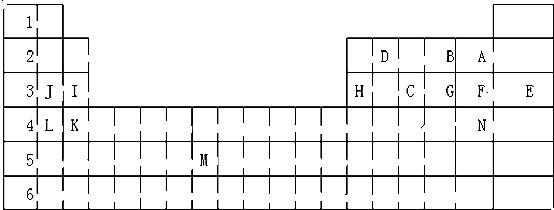
(1)元素周期表的结构
A.周期数=电子层数
B.原子序数 = 质子数
C.主族数=最外层电子数=元素最高正价数
D.主族非金属元素负价数=8-主族数
E.元素周期表结构
(2)元素周期律(强调)
A.金属元素和非金属元素的强度比较(难度)
一个。单质与水或酸反应置换氢的困难或与氢结合的困难和气态氢化物的稳定性
b.最高价氧化物水合物的碱度或酸度
c。元素还原性或氧化性的强弱
(注:元素与相应离子的性质变化规律相反)
B.元素性质随周期和组的变化
a.同一时期,元素的金属性从左到右逐渐减弱
b.同一时期,从左到右,元素的非金属性逐渐增加
c.在同一主族中,元素的金属丰度从上到下逐渐增加
d.在同一主族中,从上到下,元素的非金属性逐渐减弱
C.第三期元素变化及碱金属、卤素元素变化(包括理化性质)
D.粒子半径大小比较:
一个。原子和原子 B.原子及其离子 C.具有相同电子结构的离子
(3)元素周期律的应用(难点)
A. “位置、结构和性别”的关系
一个。原子结构决定了元素在元素周期表中的位置
b.原子结构决定元素的化学性质
c。通过位置推断原子结构和元素属性
B.预测新元素及其属性
7、化学键(重点)
(1)离子键:
A.相关概念:
B.离子化合物:大多数盐类、强碱、典型金属氧化物
C.离子化合物(AB、A2B、AB2、NaOH、Na2O2、NH4Cl、O22-、NH4+)形成过程的电子式表示(难点)
(2)共价键:
A.相关概念:
B.共价化合物:仅限非金属化合物(铵盐除外)
C.共价化合物(NH3、CH4、CO2、HClO、H2O)形成过程中的电子式表示(难点)2)
D 极性和非极性键
8、元素物质的氧化还原性
一般元素的金属性越强,其元素的还原性越强,其氧化物的阳离子氧化性越弱;
元素的非金属性越强,其元素的氧化性越强,其简单阴离子的还原性越弱。
元素位置推断法则
判断元素在元素周期表中的位置时应牢记的规则:
(1)元素周期数等于核外电子壳层数;
(2)主族元素序数等于最外层电子数。
阴阳离子半径大小的判别规则
由于阴离子是电子的最外层,所以最外层得到电子,阳离子失去电子
9、循环和主要组
周期:短周期(1—3);长周期(4—6,镧系元素存在6个周期);不完整周期(7).
主群:IA—VIIA为主群元素; IB——VIIB为亚群元素(包括中间的VIII); 0组(即惰性气体)
一般来说
(1)阳离子半径原子半径
(3)阴离子半径>阳离子半径
(4对于外电子排列相同的离子,原子序数越大,离子半径越小。
以上不适用于惰性气体!
10、对于元素周期表,从左到右,从下到上,指向整个表的右上角,元素非金属性的变化趋势是逐渐增大的。 F 氟是非金属性最高的元素(稀有气体所在的0族不包括在元素金属性和非金属性的讨论中,因此0族不适用于本规则)第一章知识点( 二)1、元素周期表一共有7个周期,3个短周期,3个长周期。第7个周期也叫不完全周期。
2、在元素周期表中,IA-VIIA是主族元素,主族和0族由短周期元素和长周期元素组成。 IB-VIIB是亚群元素,完全由长周期元素组成。
3、元素周期数=电子层数,主族元素的族数=最外层电子数,元素周期表是元素周期律的具体体现同一时期,从左到右,随着核电荷的增加,原子半径逐渐减小,原子核对核外电子的吸引力逐渐增大,元素的金属丰度逐渐减弱,非金属丰度逐渐增加。在同一主族中,从上到下,随着核电荷数的增加,原子半径逐渐增大,电子层数逐渐增加,原子核对外层电子的吸引能力逐渐减弱,元素的金属丰度逐渐增加,非金属元素逐渐增加。性功能减退。
4、元素的结构决定了元素在元素周期表中的位置,元素在元素周期表中的位置反映了原子的结构和元素的性质。我们可以根据元素在元素周期表中的位置来推断元素的结构并预测元素的性质。在元素周期表中位置相近的元素具有相似的性质,人们可以利用元素周期表来研究和合成具有特定性质的新物质。例如在金属与非金属的边界附近寻找半导体材料,在过渡元素中寻找各种优良的催化剂和耐高温耐腐蚀材料。
5、含有离子键的化合物是离子化合物;只含有共价键的化合物是共价化合物。
以电子形式表示以下物质:
CO2、N2、H2S、CH4、Ca(OH)2、Na2O2、H2O2等如:NaOH含有极性共价键和离子键,NH4Cl含有极性共价键和离子键原子结构与元素性质,Na2O2含有非极性共价键和离子键,H2O2含有极性和非极性共价键。
6、影响原子半径大小的因素:①电子层数:电子层数越多,原子半径越大(最重要的因素)
②核电荷数:核电荷数增加吸引力增大,使原子半径趋于减小(次要因素)
③核外电子数:电子数增加相互排斥力增加,使原子半径趋于增大
7、元素化合价与最外层电子数的关系:最高正价数等于最外层电子数(氟和氧元素没有正价态)
负价数=8——最外层电子数(金属元素没有负价)
8、同主群同周期元素的结构和性质:
同主族:自上而下,随着电子层数的增加,原子半径增大,吸引原子核外层电子的能力减弱,失去电子的能力增强,还原性(金属丰度)逐渐增强,而其离子的氧化性减弱。
同期:左→右,核电荷数——→逐渐增加,最外层电子数——→逐渐增加
原子半径——→逐渐减小,获得电子的能力——→逐渐增加,失去电子的能力——→逐渐减小
氧化性——→逐渐增加,还原性——→逐渐减弱,气态氢化物稳定性——→逐渐增加
最高价氧化物对应水合物的酸性——→逐渐增加,碱性——→逐渐减弱
9、判断元素金属性和非金属性的依据:
①判断元素金属丰度的依据:
易与水或酸反应置换氢气;
元素最高价氧化物的水合物——氢氧化物的碱度;置换反应。
②判断元素非金属强度的基础:
从元素和氢气中获得气态氢化物的难度和稳定性;
最高价氧化物对应的水合物的酸度;置换反应。
10、核素:具有一定数量质子和一定数量中子的原子。
①质量数==质子数+中子数:A==Z+N
②同位素:同种元素的不同原子,质子数相同,中子数不同,称为同位素。 (同一元素的各种同位素物理性质不同,但化学性质相同)。原子半径、主化合价、金属性、非金属性)随着核电荷的增加呈周期性变化规律。元素性质的周期性变化本质上是元素核外电子排列周期性变化的必然结果。
2.同时期元素性质的渐进规律
第三周期元素
11Na
12Mg
13铝
14Si
15P
16S
17Cl
18Ar
(1)电子排布
电子层数相同,最外层电子数依次增加
(2)原子半径
原子半径依次减小
—
(3)主化合价
+1
+2
+3
+4
-4
+5
-3
+6
-2
+7
-1
—
(4)金属,非金属
金属性减弱,非金属性增加
—
(5)容易用水或酸代替元素
冷水
暴力
热水和
又酸又快
与酸反应
应该很慢
——
—
(6)氢化物的化学式
——
SiH4
PH3
硫化氢
盐酸
—
(7)与H2结合的难点
——
从难到易
—
(8)氢化物稳定性
——
增强稳定性
—
(9)最高价氧化物的化学式
Na2O
氧化镁
Al2O3
二氧化硅
P2O5
SO3
Cl2O7
—
最高价的氧化物对应水合物
(10)化学式
氢氧化钠
Mg(OH)2
Al(OH)3
H2SiO3
H3PO4
H2SO4
HClO4
—
(11)酸碱
强大的基础
中等强度的基础
两性
氧化物
弱酸
中等强度
酸
强酸
很强
酸
—
(12)改变规则
碱性减弱,酸度增加
—
IA族碱金属元素:Li Na K Rb Cs Fr(Fr是金属性最强的元素,位于元素周期表的左下方)
VIIA族卤素元素:F Cl Br I At(F是最非金属元素,位于元素周期表的右上角)
★元素金属性和非金属性强弱的判断方法:
(1)金属性强(弱)——①单质容易(难)与水或酸反应生成氢气;②氢氧化物碱强(弱);③相互置换反应(强弱)Fe+CuSO4=FeSO4+Cu。
(2)非金属性强(弱)——①与氢气反应简单(困难);②生成的氢化物稳定(不稳定);③最高价氧化物的水合物(含氧酸)强(弱)酸性;④相互置换反应(强制弱)2NaBr+Cl2=2NaCl+Br2。
(一)与同期比较:
金属:Na>Mg>Al
与酸或水反应:易→难
碱性:NaOH>Mg(OH)2>Al(OH)3
非金属:Si 单质与氢的反应:从难到易 氢化物稳定性:SiH4<PH3<H2S<HCl 酸(含氧酸):H2SiO3<H3PO4<H2SO4<HClO4 (Ⅱ)与主要家族的比较: 金属性:Li 与酸或水的反应:从难到易 碱性:LiOH 非金属:F>Cl>Br>I(卤素元素) 简单物质与氢的反应:由易到难 氢化物稳定:HF>HCl>HBr>HI (Ⅲ) 金属性:Li 还原(失去电子能力):Li 氧化(电子获得能力):Li+>Na+>K+>Rb+>Cs+ 非金属:F>Cl>Br>I 氧化:F2>Cl2>Br2>I2 还原:F- 酸(厌氧酸):HF 比较粒子(包括原子和离子)半径的方法(“三观”):(1)先比较电子层数,电子层数越多半径越大。 (2)当电子壳层数相同时,再比较核电荷数,核电荷多的半径越小。
声明:文章仅代表原作者观点,不代表本站立场;如有侵权、违规,可直接反馈本站,我们将会作修改或删除处理。
图文推荐

2022-09-11 13:06:23

2022-09-11 10:57:10

2022-09-11 10:14:25

2022-09-11 09:31:29

2022-09-11 09:02:32

2022-09-11 08:48:11
热点排行
精彩文章

2022-09-11 14:02:16

2022-09-11 13:49:17

2022-09-11 13:03:02

2022-09-11 12:23:14

2022-09-11 12:23:04

2022-09-11 12:02:18
热门推荐
