
时间:2022-09-10 18:03:03来源:网络整理
本文由zhoulikt贡献ppt文档可能在WAP端浏览体验不佳。建议您优先选择TXT,或下载源文件到本机查看。专题二原子结构与元素性质第二单元原子结构与元素的性质原子核外电子排布的周期律)(原子核外电子排布的周期律)元素周期律——元素周期律是指元素性质随核电荷元素周期律是指元素性质随核电荷数递增发生周期性的递变复习回忆原子结构和性质周期性变化(1)同一周期元素结构和性质具有一定的递变性;从左到右)同一周期元素结构和性质具有一定的递变性;原子半径逐渐减小,失电子能力逐渐减弱,得电子能力逐渐,元素的金属性逐渐减弱非金属性逐渐增强,对应氢化物的稳定性逐渐增强高价氧化物对应的水化物的酸性逐渐增强;碱性逐渐减弱(2)同一主族元素结构和性质具有一定的相似性和递变性;)同一主族元素结构和性质具有一定的相似性和递变性;同一主族,从上到下:原子半径逐渐增大,失电子能力同一主族,从上到下:逐渐增强得电子能力逐渐减弱,金属性逐增强,非金属性逐渐减弱;对应氢化物的稳定性减弱;最高价氧化物对应的水化物的酸性逐减弱;碱性逐渐增强原子核外价电ns1ns2ns2np1ns2np2ns2np3ns2np4ns2np5子排布最高正价+1+2+3+4+5+6+7最低负价-4-3-2-1最高正价:+1+7;最低负价:4:+1+7;最低负价化合价变化最高正价:+1+7;最低负价:-4-1金属性和非金属性变化原子半径变化规律金属性减弱非金属性增强同周期从左到右半径逐渐减小原子核外电子排布的周期性周期元素外围电子排布最多可容纳的1s11s22s12s22p63s13s23p6184s14s24p6185s15s25p66s16s26p6随着原子序数的增加,随着原子序数的增加,元素原子的外围电子排布呈现周期性的变化:电子排布呈现周期性的变化:每隔一定数目的元素,元素原子的外围每隔一定数目的元素,电子排布重复出现从ns电子排布重复出现从ns1到ns2np6的周期性变思考与探究按照电子排布,可把周期表的元素划分为5按照电子排布,可把周期表的元素划分为5区。
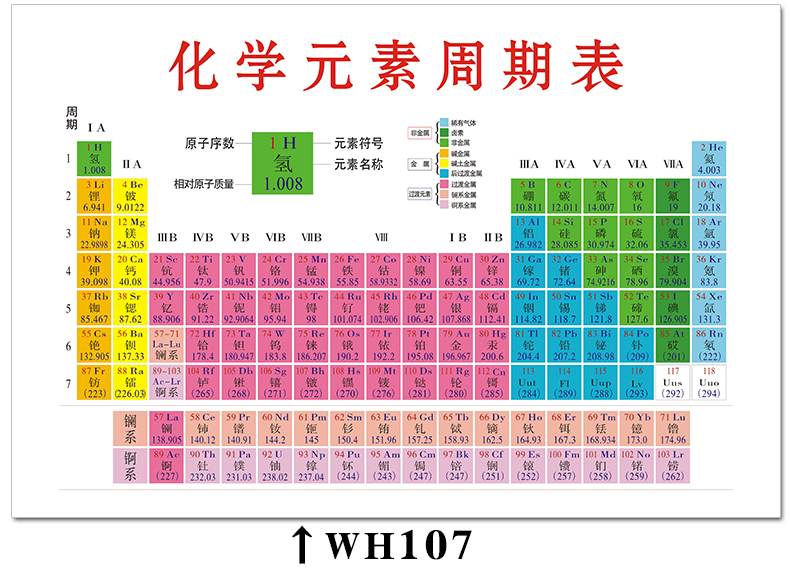
划分区的依据是什区分别有几个纵列?区分别有几个纵列?区的名称来自按照构造原理最后填充的能级的符号区的名称来自按照构造原理最后填充的能级的符号区元素最后1轨道上,最后1个电子填充在ns轨道上,价电子位于周期表的左的构型是ns1或ns2,位于周期表的左侧,包它们都是活泼金属容易失活泼金属,族,它们都是活泼金属,容易失电子形成+1+2价离子价离子。去电子形成+1或+2价离子。区元素最后个电子填充在np轨道上,价层电最后轨道上,位于周期表右子构型是ns2np1~6,位于周期表右侧原子结构与元素性质,包族元素大部分为非金属族元素。非金属。稀有气体也属于p稀有气体也属于p区的共同特点是:最后1个电子都排布在最外层最外层电子的总数等于最外层,都排布在最外层,最外层电子的总数等于该元素的族序族序数该元素的族序数。s区和p区就是按族划分的周期表中的主的周期表中的主族0族。区元素它们的价层电子构型是(它们的价层电子构型是(n-1)d1~9ns1~2,最后1最后1轨道上的元素位于长周期的中轨道上的元素,轨道上的元素,位于长周期的中部。这些元素都是金属常有可变化合价金属,可变化合价,这些元素都是金属,常有可变化合价,称为过渡元素。
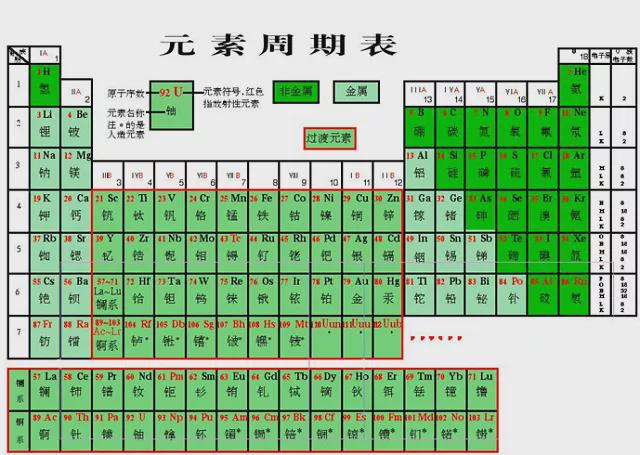
它包括B族元素。过渡元素。它包括B~族元素。ds区元素ds区元素价层电子构型是(价层电子构型是(n-1)d10ns1~2,即次外层轨道是充满充满的最外层轨道上有次外层轨道是充满的,最外层轨道上有个电子。它们既不同于个电子。它们既不同于s区,也不同故称为dsds称为ds区,它包括B区之间。它们都是金属金属,处于周期表d区之间。它们都是金属,也属过渡元素过渡元素。也属过渡元素。区元素最后1个电子填充在f轨道上原子结构与元素性质,最后1个电子填充在f轨道上,价电子构镧系和锕系元素(n-1)d0~2ns2,它包括镧系和锕系元素(各有14种元素)。各有14种元素)。14种元素小结各区元素特点包括元素价电子排布化学性质ns1、ns2活泼金属ns2np1~6(n-1)d10ns1~2过渡元素n-2)f0~14ns2思考:为什么区、ds区的元素都区的元素都是金属(除区、ds区的元素最外层电子数为1ds区的元素最外层电子个电子,在反应中易失去,所以都是金个电子,在反应中易失去,思考:思考:为什么副族元素又称为过渡元素?为什么副族元素又称为过渡元素?2.为什么在元素周期表中非金属元素主要集中在为什么在元素周期表中非金属元素主要集中在右上角三角区内(如图)?)?处于非金属三角区边右上角三角区内(如图)?处于非金属三角缘的元素常被称为半金属或准金属。
为什么?缘的元素常被称为半金属或准金属。为什么?为什么副族元素又称为过渡元素?为什么副族元素又称为过渡元素?副族元素处于金属元素向非金属元素过渡的区域,因此,又把副族元素称为过渡元素。过渡元素区域,因此,又把副族元素称为过渡元素。2.为什么在元素周期表中非金属元素主要集中在右上角为什么在元素周期表中非金属元素主要集中在右上角三角区内(如图)?)?处于非金属三角区边缘的元素常被三角区内(如图)?处于非金属三角区边缘的元素常被称为半金属或准金属。为什么?称为半金属或准金属。为什么?这是由元素的价电子结构和元素周期表中元素性质递变规律决定的,在元素周期表中,规律决定的,在元素周期表中,同周期的元素从左到右非金属性渐强,同主族元素从上到下非金属性渐弱,非金属性渐强,同主族元素从上到下非金属性渐弱,结果使元素周期表右上角的元素主要呈现非金属性。果使元素周期表右上角的元素主要呈现非金属性。处于非金属三角区边缘的元素既能表现出一定的非金属性,又能表现出一定的金属性,因此,的非金属性,又能表现出一定的金属性,因此,这些元素常被称之为半金属或准金这些元素常被称之为半金属或准金属。课堂小结:课堂小结一、原子结构与元素周期表1、原子的电子排布与周期的划分周期序数=能层数周期序数能层数2、原子的电子排布与族的划分主族元素:族序数=原子的最外层电子数主族元素:族序数==价电子数元素:大多数族次=1)d+ns电子数=电子数=价电课堂练习已知某元素的原子序数为25,25,试写出该元素原子的电子排布式,排布式,并指出该元素在周期表中所属周期、族和区。

表中所属周期、族和区。课堂练习5、已知某元素在周期表中位于第五周期、A已知某元素在周期表中位于第五周期、位置上。试写出该元素基态原子的价电子族位置上。试写出该元素基态原子的价电子排布式、电子排布式并分析该元素在哪区?排布式、电子排布式并分析该元素在哪区? 由于是A 4d必是全充满的, 4d 必是全充满的 必是全充满的, 由于是A 所以价电子排布为5s所以价电子排布为5s25p4, 电子排布式 [Kr]4d105s25p4 练习:练习: 1.已知一元素的价层电子结构为3d 1.已知一元素的价层电子结构为3d54s2,试 已知一 元素的价层电子结构为 确定其在周期表中的位置。 确定其在周期表中的位置。 第四周期, 2.试确定32号元素在周期表中的位置。 2.试确定32 号元素在周期表中的位置。 确定32号元素在周期表中的位置 第四周期,A 3.判断处于第三周期,A族元素的价 3.判断处于第三周期,A族元素的价层 判断处于第三周期 电子结构、原子序数。 子结构、原子序数。[Ne]3s23p2,第14 号元素
声明:文章仅代表原作者观点,不代表本站立场;如有侵权、违规,可直接反馈本站,我们将会作修改或删除处理。
图文推荐

2022-09-10 17:24:13

2022-09-10 16:04:23

2022-09-10 15:58:34

2022-09-10 15:58:15

2022-09-10 15:15:02

2022-09-10 14:32:06
热点排行
精彩文章

2022-09-10 18:03:03

2022-09-10 17:24:25

2022-09-10 17:05:08

2022-09-10 17:03:50

2022-09-10 15:58:37

2022-09-10 14:32:29
热门推荐
