
时间:2022-07-17 15:04:22来源:网络整理
电化学基础第三讲.docx
上传者:t*** 文档ID:7339290 上传时间:2022-06-16 格式:DOCX 页数:16 大小:261.06KB
电化学基础第三讲
2010年高考总评-化学3
电化学基础
电化学知识是历年高考的重要组成部分。主要测试点有:
原电池和电解池的电极判断及电极反应公式的编写;根据原电池和电解槽的电极变化判断金属活性;根据电解过程中电极的变化判断电极材料或电解液类型;新型电池的电极反应及应用;电解产物的判断和计算。
原电池的工作原理、电解产品的判断与计算是高考命题的热点。
试题主要涉及电极反应、溶液pH变化、金属活度判断、相关定量计算等。主要题型包括选择题、简答题、综合分析计算题等。
高考中,电化学的基础知识出现的频率很高。究其原因,一是这部分知识在现实生活和工业生产中具有极其重要的地位和作用;另外就是这部分知识的综合程度很高,除了有机化学,还涉及到高中化学的基本概念、基础理论、元素化合物知识、化学计算、化学实验等方面。候选人的知识和能力都非常高。
展望未来,命题将继续在上述方面进行。同时,新能源、环保、工业生产等热点问题,以及利用电解原理实现普通方法难以制备的物质的实现。
原电池和电解池的本质是发生在电极上的氧化还原反应,是氧化还原反应的进一步延伸和深化。
这部分知识既有化学实验验证,又有理论分析推理过程。
由于电化学经常涉及到串联电路、并联电路以及物理学中相关的物理量,如电流、电压、电阻、时间、电荷等,因此也要求学生具备一定的物理知识基础。
毫不夸张地说,电化学知识能否掌握好,可以充分体现考生在化学乃至自然科学领域的知识水平和能力水平。
高考电化学的具体要求如下:
①了解原电池和电解槽的工作原理。
②能够结合氧化还原、离子反应及相应元素化合物的知识,准确判断电极上发生的化学反应,写出电极反应和电池反应方程式。
③了解常用化学电源的种类及其工作原理。
④了解铜电解精炼、镀铜、氯碱工业的反应原理。
⑤了解金属电化学腐蚀的原因、金属腐蚀的危害以及防止金属腐蚀的措施。
热点一、日常生活中使用的充电电池分析
1、化学电源在日常生活和工业生产中有着广泛的用途,所以越来越多的关于原电池的知识在高考中被考查,主要集中在利用原电池的原理分析生活中的电池(尤其是新电池、燃料电池)。
基本思路:
①根据一次电池的原理和元素化合价的变化来判断电极。
②根据题目写出原电池反应的一般方程,并写出某个电极的电极反应方程。
在编写电极反应方程和一般方程时电解还原水生成器电路,必须注意除了氧化还原过程(电子转移)之外,还必须考虑溶液中溶质的参与(离子反应)。
③从电池反应的一般方程和已经写好的电极反应公式中“减去”另一个电极的电极反应公式。
规则:
先写出自己比较熟悉的电极反应式,再根据条件写出通式,最后从通式中“减去”写好的电极反应式,得到另一个不常见的电极反应式。
例子:
甲烷燃料电池、电解液:
强碱 (KOH) 溶液
先写出O2所在的电极——正极的反应式:
2O2+8e-+4H2O=8OH-;
然后写出一般方程:
CH4+2O2+2OH-=CO32-+3H2O(由于溶液中存在大量OH-,不能生成CO2)
最后得到负极的反应式:
CH4-8e-+10OH-=CO32-+7H2O
④由于日常生活中二次电池的广泛使用,二次电池的放电过程利用一次电池反应,充电过程利用电解池反应。注意这两种设备的区别。
原电池
电解槽
设备的本质
两极发生氧化还原反应,
产生电流以将化学能转化为电能
在直流电的作用下,发生在两极上
氧化还原反应,将电能转化为化学能
电子流
方向
电子从负极流向正极
电子从直流电源的负极流出,然后通过导线到达电解槽的阴极,然后离子通过电解液到达阳极,离子在阳极失去电子, 电子返回直流电源正极
在电极上
反应
否定:
还原剂失去电子,发生氧化反应
正面:
氧化剂获得电子并发生还原反应
阳极:
发生氧化。
如果是惰性电极,溶液中的阴离子会失去电子;如果是活性电极,阳极本身会失去电子
阴极:
发生还原反应。
阴极本身只起传递电子的作用,溶液中的阳离子得到电子并发生还原反应
例1(08高考)。电池是人类生产生活中重要的能源。各种电池的发展是化学对人类的重大贡献。
下列关于电池的说法正确的是()
A.锌锰干电池工作一段时间后碳棒变细
B.氢氧燃料电池可以直接将热能转化为电能
C.氢氧燃料电池工作时氢气在阳极被氧化
D.太阳能电池的主要材料是高纯二氧化硅
分析:
方案A中,锌锰干电池作为负极,石墨作为电池正极,仅起导电作用,被锌腐蚀;方案B中,氢氧燃料电池直接将化学能转化为电能。而不是直接将热能转化为电能;太阳能电池的主要材料是高纯单晶硅,具有很高的能量转换率。
答案:
C
例2(08高考)。 LiFePO4电池具有稳定性高、安全、环保等优点,可用于电动汽车。
电池响应为:
FePO4+LiLiFePO4,电池正极材料为LiFePO4,负极材料为石墨,含有Li+的导电固体为电解质。
下列关于磷酸铁锂电池的说法正确的是()
A.可添加硫酸以提高电解液的电导率
B.电池中的Li+在放电时向负极移动
C.在充电过程中,电池正极材料的质量减少
D.电池放电时的正极反应为:
FePO4+Li++e-=LiFePO4
分析:
放电时,负极:
Li-e—=Li+,正极:
FePO4+Li++e—=LiFePO4;充电时,阳极:
LiFePO4-e—=FePO4+Li+,阴极:
Li++e—=Li,所以 C 和 D 是正确的。
如果加入硫酸,它会与锂元素(固体)反应,所以A是错误的;放电时,Li+(正电荷)应该移动到电池内部(电解液中)的正极,所以B是错误的。
答案:
光盘
例3(08高考)。镍镉(Ni-Cd)充电电池在现代生活中应用广泛。
已知镍镉电池的电解液为KOH溶液,其充放电过程如下:
Cd+2NiOOH+2H2OCd(OH)2+2Ni(OH)2
关于电池的正确说法是()
A.充电时的阳极反应:
Ni(OH)2-e—+OH—=NiOOH+H2O
B.充电过程就是将化学能转化为电能的过程
C.放电时靠近负极的溶液碱度保持不变
D.放电时电解液中的OH-向正极移动
分析:
从充电过程中等式中Cd和Ni的化合价变化可以看出,以Ni(OH)2为阳极,电解液为KOH,因此电极反应式为:
Ni(OH)2-e-+OH-=NiOOH+H2O; Cd(OH)2作阴极,Cd(OH)2+2e-=Cd+2OH-;充电的过程就是将电能转化为化学能。
放电时以Cd为负极,Cd-2e-+2OH-=Cd(OH)2,Cd周围的c(OH-)减少,OH-向负极移动。
答案:
一个
例4(09高考)。市面上常见的标有锂离子的电池称为“锂离子电池”。
负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解液是可以导电Li+的高分子材料。
这种锂离子电池的电池反应是:
下列说法不正确()
A.放电时,负极的电极反应式为:
Li-e—=Li+
B.充电过程中,Li0.85NiO2同时发生氧化和还原反应
C.电池不能使用水溶液作为电解液
D.放电时Li+向负极移动
答案:
D
例5(09高考)。 Li-SOCl2 电池可用于心脏起搏器。
该电池的电极材料分别为锂和碳,电解液为LiAlCl4-SOCl2。
电池的总反应可表示为:
4Li+2SOCl2=4LiCl+S+SO2。
请回答以下问题:
(1)电池的负极材料是,发生的电极反应是;
(2)电池正极处的电极反应为;
(3)SOCl2易挥发,实验室常用NaOH溶液吸收SOCl2,生成Na2SO3和NaCl。
如果将少量水滴入SOCl2中,实验现象是反应的化学方程式为;
(4)这个电池的组装必须在无水无氧条件下进行,原因是。
答案:
(1)锂Li-e—=Li+
(2)2SOCl2+4e—=4Cl—+S+SO2
(3)出现白雾并产生刺激性气体;SOCl2+H2O=SO2↑+2HCl↑
(4)锂是活泼金属,易与H2O和O2反应;SOCl2也可与水反应
2、燃料电池是研究热点,在工业生产中具有广阔的应用前景。
与传统的原电池不同,燃料电池利用某些金属材料对气体的良好吸附性能,使气体在金属电极表面发生氧化还原反应。
燃料电池所用的原材料很容易获得,但与传统电池相比,维护成本高,使用时存在安全问题。
在回答燃料电池问题时,要求考生对原电池的形成条件有深入的了解:
(1)还原剂和氧化剂在两个不同的电极上发生反应(在反应中,还原剂和氧化剂的粒子不发生直接有效碰撞反应,否则不能形成电流)。
(2)形成一个闭合回路,两个电极通过导线连接(或直接接触)。
在电池内部,两个电极之间应填充导电介质(通常为电解质,但在某些电池中,由于电极与水发生剧烈反应,因此不能使用水溶液)。
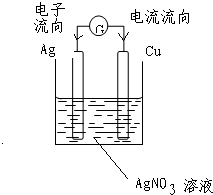
例6(08高考)。用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(U型管内填充琼脂-KNO3))构建原电池。
下列关于原电池的说法正确的是()
①在外电路中,电流从铜电极流向银电极
②阳性反应是:
Ag++e-=Ag
③实验过程中去除盐桥,原电池继续工作
④将铜片浸入AgNO3溶液中的化学反应与原电池相同
A. ①②B. ②③C. ②④D. ③④
分析:
Cu为负极,Ag为正极。
否定:
Cu-2e—=Cu2+;正极:
Ag++e—=Ag。
在外电路中,电子从Cu电极流向Ag电极,电流方向与电子方向相反,所以①错误。
没有盐桥,原电池无法继续工作,③错。
不管是不是原电池,反应本质上都是一样的,都是氧化还原反应,④是的。
答案:
C
例7(09高考)。控制合适的条件,将反应2Fe3++2I—=2Fe2++I2设计成如下图所示的原电池。
下列哪项是错误的()
A.反应开始时,B中石墨电极发生氧化反应
B.反应开始时,A中石墨电极上的Fe3+被还原
C.当电流计读数为零时,反应达到化学平衡状态
D.电流计读数为零后,FeCl2固体溶解在A中,B中的石墨电极为负极
答案:
D
例8(08高考)。燃料电池中发生的化学反应是:
甲醇在酸性溶液中与氧气反应生成水和二氧化碳。
电池负极的反应是()
A. CH3OH(g)+O2(g)=H2O
(1)+CO2(g)+2H+(aq)+2e-
B. O2(g)+4H+(aq)+4e-=2H2O
(1)
C. CH3OH(g)+H2O
(1)=CO2(g)+6H+(aq)+6e-
D. O2(g)+2H2O
(1)+4e-=4OH-
分析:
甲醇与氧气反应的化学方程式为:
2CH3OH+3O2→2CO2+4H2O,所以甲醇失去电子在负极上放电。该电极上的电极反应式为:
CH3OH(g)+H2O
(1)=CO2(g)+6H+(aq)+6e-.
答案:
C
例9(09高考)。以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。
关于电池的说法是正确的()
A.电池可在高温下工作
B.电池的负极反应为:
C6H12O6+6H2O-24e—=6CO2↑+24H+
C.在放电过程中,H+从正极区迁移到负极区
D.在电池反应中,标准条件下每消耗1mol氧气理论上可以产生气体
答案:
B
例10(09高考)。氢氧燃料电池是一种符合绿色化学理念的新型发电装置。
下图是电池的示意图。电池的电极表面涂有一层精细的铂粉。铂具有很强的气体吸附能力和稳定的性能。请回答:
(1)氢氧燃料电池中能量转换的主要形式是导线中电子流动的方向是(用a,b表示)。
(2)负反应公式为。
(3)电极表面涂铂粉的原因是。
(4)电池工作时,不断从外部供给H2和O2,电池可以持续供电。
因此,大量安全储氢是关键技术之一。
锂金属是一种重要的储氢材料。氢气的吸脱附原理如下:
Ⅰ. 2Li+H22LiH
Ⅱ. LiH+H2O=LiOH+H2↑
①反应Ⅰ是还原剂,反应Ⅱ是氧化剂。
②LiH的已知固体密度为0.82g/cm3。
用锂吸收224L(标准条件)H2,生成的LiH体积与吸收的H2体积之比为。
③②产生的LiH与H2O相互作用,释放的H2用作电池燃料。如果能量转换率为80%,则通过导线的电子量为mol。
答案:
(1)从a到b从化学能到电能
(2)2H2+4OH--4e-=4H2O或H2+2OH-2e-=2H2O
(3)增加电极单位面积吸附的H2、O2分子数,加快电极反应速率
(4)①LiH2O②1/1148或8.71×10-4③32
例11。X、Y、Z、W是四个短周期元素,按原子序数升序排列。
已知:
①X可以分别与Y、W形成X2Y、X2Y2、XW等共价化合物; ②Z可以分别与Y和W形成Z2Y和Z2Y2、ZW等离子体化合物。
请回答:
(1)Z2Y的化学式是。
(2)Z2Y2与X2Y反应的化学方程式为。
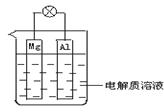
(3)如图所示,两根玻璃管内填充有酚酞溶液的ZW饱和溶液,C(I)和C(II)为多孔石墨电极。
开启S1后,C(I)附近的溶液变红,两个玻璃管内产生气体。
一段时间后(两个玻璃管内的液位没有离开电极),断开S1,打开S2,电流表指针偏转。
此时:
C(I)的电极名称为(填正极或负极);
C(II)的电极反应式为。
(4)铜屑在稀硫酸中不会发生反应。如果在稀硫酸中加入X2Y2,铜屑会逐渐溶解。反应的离子方程式为。
答案:
(1)Na2O
(2)2Na2O2+2H2O=4NaOH+O2↑
(3)负Cl2+2e-=2Cl-
(4)Cu+H2O2+2H+=Cu2++2H2O
热点二、电解知识结合实验计算
1、电解槽内的材料在电流作用下发生氧化还原反应,广泛应用于金属冶炼、材料制备、污水处理等工业领域。
在最近的高考中,电解原理很少被考查,而是经常与化学实验或计算相结合。 ,解决真正的问题。
例12(08高考)。取一张浸泡在饱和NaCl溶液中的pH试纸,用两根铅笔芯作为电极,打开直流电源。一段时间后,发现a电极与试纸接触处出现一个双色同心圆,内圈为白色,外圈为白色。淡红色。
以下说法为假()
A. b电极是阴极b。 a电极接电源正极
C.水是电解过程中的氧化剂 D. b 电极附近溶液的 pH 值降低
分析:
本题选自教材中的氯化钠溶液电解演示实验。 a电极与试纸接触处出现双色同心圆。极接电源正极,即a为阳极,电极反应式为:
2Cl--2e-=Cl2↑,b为阴极,2H2O+2e-=H2↑+2OH-,故b极附近的pH值升高。
答案:
D
例13(07高考)。一个课外小组对一些金属和化合物的性质进行研究。
(1)下表为《铝与氯化铜溶液的反应》实验报告的部分内容:
实验步骤
实验现象
将抛光后的铝片(过量)放入一定浓度的CuCl2溶液中
形成气泡,析出松散的红色固体,溶液逐渐变为无色
反应完成后,分离出溶液备用
红色固体用蒸馏水洗涤后置于潮湿空气中
一段时间后固体由红色变为绿色[取决于其主要成分为Cu2(OH)2CO3]
根据反应类型为实验中的每个反应写一个化学方程式(离子反应的唯一离子方程式)
置换反应;
组合反应。
(2)以石墨为电极,电解上述实验分离的溶液,两极产生气泡。
连续电解,在靠近阴极的溶液中也可以观察到这种现象。
解释这种现象的离子方程是。
答案:
(1)2Al+6H+=2Al3++3H2↑或2Al+3Cu2+=2Al3++3Cu
2Cu+O2+H2O+CO2=Cu2(OH)2CO3
(2)形成白色沉淀,后者逐渐溶解消失;Al3++3OH-=Al(OH)3↓;Al(OH)3+OH-=AlO2-+2H2O
例14(09高考)。在下图所示的装置中,三个烧杯 A、B、C 分别装满 100g5.00% NaOH 溶液、足量的 CuSO4 溶液和 100g10.00% K2SO4 溶液。都是石墨电极。
(1)接通电源,一段时间后测得C中的K2SO4浓度为10.47%,B中电极C的质量增加了。
相应地回答问题:
①电源的N端为极;
②电极b上的电极反应为;
③用柱式计算标准状态下电极b产生的气体体积:
;
④电极c的质量变化为g;
⑤电解前后各溶液酸碱度是否发生变化,并简述原因:
一个解决方案;
B 解决方案;
C 解;
(2)如果电解过程中铜全部析出,电解还能继续吗?为什么?
分析:
(1)①电极C在B中的质量增加,c处的反应为:
Cu2++2e-=Cu,即C为阴极。由此可以推导出b为阳极,a为阴极,M为负极,N为正极。
C是K2SO4,相当于电解水。设电解水的质量为xg。
电解前后溶质质量相等:
100×10%=(100-x)×10.47%,所以x=4.5g,所以是0.25mol。
从方程2H2+O2=2H2O可以看出,生成了2molH2O,转移了4mol电子,所以整个反应转移了0.5mol电子,整个电路串联起来,所以每个烧杯中电极上转移的电子数是相等的。
②A为NaOH,相当于电解H2O,阳极b为阴离子OH-放电,即4OH--4e-=2H2O+O2↑。
③转移0.5mol电子,则生成的O2为0.5/4=0.125mol,标准条件下体积为0.125×2 2.4=2.8L.
④Cu2++2e-=Cu,转移0.5mol电子,则生成m(Cu)=0.5/2×64=16g。
⑤A相当于电解水,因此NaOH浓度增加,pH值增加。
B中,阴极为Cu2+放电,阳极为OH-放电,H+升高,pH降低。
C为电解水,其pH值对K2SO4几乎不变。
(2)铜全部析出电解还原水生成器电路,H2SO4可连续电解,有电解液即可电解。
答案:
(1)①正极②4OH--4e-=2H2O+O2↑③2.8L④16g⑤A增加,因为相当于电解水;B减少,OH-放电,H+增加;C不变,相当于电解水。
(2)由于CuSO4溶液已经转化为H2SO4溶液,反应也会变成水的电解反应。
2、电解原理在工业生产中有重要应用。工业生产中,电解前需要先对原料进行提纯,离子反应和实验设计难免受到审查;工业生产追求经济效益,会跟计算有关系;而现代工业“可持续发展”的方向,必须能够评价和改进现有的工业生产原则,还要与环境保护相结合;工业生产中的电解精炼和电镀。相关生产涉及使用非惰性电极。
因此,在高考中,一旦出现涉及工业生产的题目,其综合性远超其他题目。
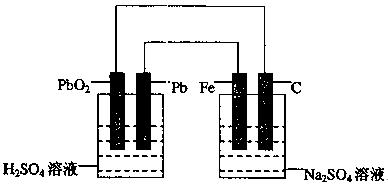
例15(07高考)。一名学生使用下图所示的装置进行电解实验。
下列哪项是正确的
A.电解过程中,铜电极上会产生氢气
B.电解初期,主要反应方程式为:
Cu+H2SO4CuSO4+H2↑
C.电解一定时间后,石墨电极上析出铜
D.在整个电解过程中,H+的浓度不断增加
答案:
公元前
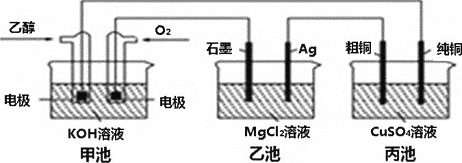
例16(09高考)。请回答以下氯碱行业的问题:
(1)氯气和烧碱是盐水电解过程中以固定比例k(质量比)产生的产物。
理论上k =(需要计算表达式和结果);
(2)原盐中常含有沉淀物和杂质,如Ca2+、Mg2+、Fe3+、SO42-等,必须经过精制后才能用于电解。
精制时,粗盐溶于水过滤后,加入的试剂为①Na2CO3、②HCl(盐酸)③BaCl2,这三种试剂的合理加入顺序为(填写序列号)数)
(3)氯碱行业是高耗能行业,电解电池和燃料电池相结合的新工艺可以节省(电)能源30%以上。
在本工艺设计中,相关材料的传输与转化关系如下图所示,其中电极未标注,所用离子膜只允许阳离子通过。
①图中X和Y分别为,(填化学式),分析比较图中氢氧化钠的质量分数a%和b%;
②分别写出燃料电池正负极上的电极反应
正面:
;否定:
;
③本设计的主要节能(电)在于(写2处),.
答案:
(1)k=M(Cl2)/2M(NaOH)=71/80=1:1.13 或 0.89
(2)③①②
(3)①Cl2H2a%小于b%②O2+4e-+2H2O=4OH-H2-2e-+2OH-=2H2O③燃料电池可以补充电解槽消耗的电能;增加浓度输出碱液;降低能耗
例17(09高考)。新型锂离子电池在新能源发展中发挥着重要作用。
可用作节能环保电动汽车的动力电池。
磷酸铁锂(LiFePO4)是新型锂离子电池的首选电极材料,其制备方法如下:
方法一:
Lithium carbonate, ferrous acetate [(CH3COO)Fe] and ammonium dihydrogen phosphate are mixed in a certain proportion, fully ground, and then calcined at about 800 ℃ in an inert gas atmosphere to obtain crystalline lithium ferrous phosphate. The resulting acetic acid and other products escape as gases.
方法二:
A certain concentration of ammonium dihydrogen phosphate and lithium chloride mixed solution is used as the electrolyte, the iron rod is used as the anode, and the graphite is used as the cathode, and the lithium ferrous phosphate precipitate is electrolytically desorbed.
The precipitate is filtered, washed, dried, and calcined at about 800°C in an inert gas atmosphere to obtain crystalline lithium ferrous phosphate.
In lithium ion batteries, an organic polymer is required as a medium for lithium ion transfer between positive and negative electrodes. The structural formula of one of the monomers of the organic polymer (represented by M) is as follows:
Please answer the following questions:
(1)The above two methods of preparing lithium iron phosphate must be carried out in an inert gas atmosphere.
The reason is.
(2)In the reaction of method 1, in addition to the formation of lithium iron phosphate and acetic acid, there are also formations of , , (fill in the chemical formula).
(3)In method 2, the electrode reaction formula of the anode to generate lithium iron phosphate is:
.
(4)Write the chemical equation for the reaction of M with a sufficient amount of sodium hydroxide solution:
.
(5)It is known that during the charging process of the lithium-ion battery, the lithium ferrous phosphate of the anode generates iron phosphate, and the electrode reaction formula of the positive electrode when the battery is discharged is as follows.
答案:
(1)In order to prevent ferrous compounds from being oxidized
(2)CO2H2ONH3
(3)Fe+H2PO4—+Li+2e=LiFePO4+2H+
(4)
(5)FePO4+Li++e=LiFePO4
Example 18 (08 college entrance examination). Salt is a necessities of daily life and an important chemical raw material.
(1)Coarse table salt often contains a small amount of impurity ions such as K+, Ca2+, Mg2+, Fe3+, SO42-, etc. The process of purifying NaCl in the laboratory is as follows:
Reagents provided:
Saturated Na2CO3 solution, saturated K2CO3 solution, NaOH solution, BaCl2 solution, Ba(NO3)2 solution, 75% ethanol, carbon tetrachloride
①To remove Ca2+, Mg2+, Fe3+, SO42- ions in solution I, select the reagent represented by a, and the order of dropping is _______ (only fill in the chemical formula).
②Wash to remove a small amount of KCl attached to the surface of the NaCl crystal, and the selected reagent is _________.
(2)Use purified NaCl to prepare 500mL4.00mol·L-1NaCl solution. The instruments used include (fill in the name of the instrument) in addition to the medicine spoon and glass rod.
(3)The device for electrolyzing saturated brine is shown in the figure, if the collected H2 is 2L, then the Cl2 collected under the same conditions (fill in ">", "=" or "
声明:文章仅代表原作者观点,不代表本站立场;如有侵权、违规,可直接反馈本站,我们将会作修改或删除处理。
图文推荐

2022-07-17 12:10:32

2022-07-17 10:10:25

2022-07-16 14:01:05

2022-07-15 17:23:18

2022-07-15 16:01:29

2022-07-15 15:02:43
热点排行
精彩文章

2022-07-17 15:04:22
2022-07-17 15:03:48

2022-07-17 13:06:32

2022-07-17 09:07:10

2022-07-16 16:05:06
2022-07-16 16:03:54
热门推荐
