
时间:2022-05-02 14:00:27来源:网络整理
根据电化学腐蚀理论,金的溶解反应主要取决于金粒微电池的反应电动势(E)。 E值越大,金溶解反应的自由能变化(ΔG=-nFE)越小,反应的驱动力越大,金溶解反应的热力学条件越好。也就是说,为了加速金在溶液中的氧化溶解反应,需要增大正负极反应的电位差(电动势)。采用浸金时,负极Au的反应电位(SCN2H4)2+∕Au对0.38V(25℃时)是一个定数,只要氧化剂高成对电位用于增加正极响应 正负反应之间的电位差可以扩大,在酸性溶液中具有恢复性。要使金溶解到溶液中,还必须存在氧化剂。选择氧化剂时,首先考虑的应该是它的价格低,易得,回收产物不满足形成稳定络合物等条件,还应该考虑它的电位要高于负极金的反应电位和银溶解络合离子。一般来说抗铜剂mda5与抗氧剂168混合是啥抗氧剂f,氧化剂的电位越高,金银溶解反应越好。功率越大,功率越大。但氧化剂的氧化能力氧化剂过强抗铜剂mda5与抗氧剂168混合是啥抗氧剂f,会加剧氧化,分化为S0、HSO4-、SO42-等,增加消耗,甚至失效。表1是一些常用氧化剂的标准氧化恢复电位。 И.Н. Praxine在浸金实验中分别使用了漂白剂、重氧化剂。实验中发现溶液中金的溶解量很小,很快就出现了元素硫的沉积。解释这些氧化剂的作用。氧化能力太强,会很快被氧化分化。此外,只能从具有中等电位的高价铁盐、氧气和二氧化锰等氧化体系中选择。
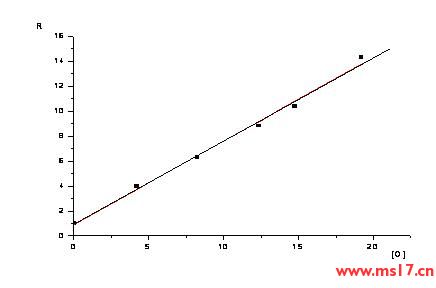
表1 常用氧化剂标准氧化还原电位@1.396<@1.385<@1.333对O3∕H2OMnO2∕Mn2+NO3-∕HNO2Fe3-∕Fe2+SO42∕H2SO3E0∕V1.@ >228<@1.2280.@ >940.720.420.17 由于金矿石和精矿总是含有一些铁(黄铁矿、褐铁矿等),在酸浸过程中,必须将一部分铁溶解到溶液中,这为使用Fe3+作为氧化剂提供了条件。而在正常操作条件下,溶液中的铁0.5~0.6@>0g∕L可以作为氧化剂,所以在浸出矿石或精矿时,只需将其吹入浸出液中即可。解决方案。溶解在溶液中的氧气可以将Fe2+氧化成Fe3+,Fe3+不断再生。而吹压缩空气溶解在溶液中的氧气浓度约为0.7@>2mg∕L,其本身就足以将金氧化成溶液(公式0.8@>。因此,Fe3+和爆破溶解的氧气为用作混合氧化剂,有利于提高浓度,金颗粒表面不会被钝化,可强化浸出过程,因此成为当今浸金最理想的氧化剂。@1)As如上所述,金微电池的反应电动势(E)等于正负反应电位差(E=φ+-φ-)。
以Fe3+为氧化剂时,反应式(2)~(4))的反应电位和电动势分别为:Fe3++e Fe2+ (2)Au++2SCN2H4 Au(SCN2H4)2+ (3)Au+Fe3++2SCN2H4 Au(SCN2H4)2++Fe2+ (4)公式(2)电位φ+=Fe3+∕Fe2+=0.77V公式)(3)电位φ-=Au(SCN2H4)2+∕Au=0.38V型(4)电动势E=φ+-φ-=0.39V可见由上式可知,使用Fe3+作为氧化剂溶金,其浸出反应电动势高,完全可以满足作为氧化剂溶金的要求,而且价格便宜,易得。 (SCN2H3)2/SCN2H4对为0.42V,(3)Au(SCN2H4)2+/Au对)0.38V为高0.04V。因此,在溶解金的过程中,二硫化甲脒也成为氧化剂参与金的氧化。并且在pH1~<@1.5的范围内,二硫化物甲脒生成银的作用比金强。但与正常情况下的Fe3+相比,二硫代甲脒的氧化作用仍然很小。 2SC (NH2)2 (SCN2H3)2+2H++2e (1.5@>然而,R.G. Schulze 的实验得出了相反的结果。他使用了一个 0.25cm2 重 4 5.8mg, 1L 5 颈玻璃反应釜中,pH=<@1.0、浓度0.5g∕L,温度40℃,搅拌速度400r条件下/min,加入不同浓度的Fe3+作为氧化剂进行金的浸出,发现只有当Fe3+的浓度为0.2~0.7g∕L时,金的溶解速度加快随着Fe3+浓度的增加。
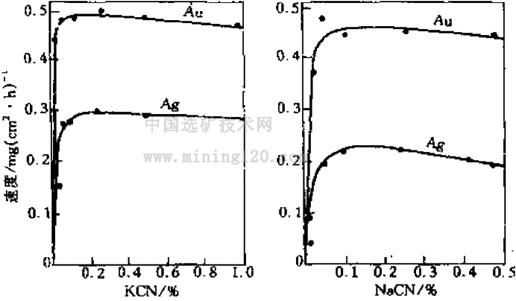
当Fe3+浓度达到或超过3g/L时,金的溶解速率随着浸出时间的延长而降低。这可能是由于Fe3+浓度增加引起的氧化损失所致。图1为不同Fe3+浓度下不同时间溶解金量的变化曲线。从图中可以看出,实验曲线呈现出相交现象。如果用图中3h、6h、7h的数值来评价实验结果,会得出相反的结论。这一现实之所以被众多研究人员所忽视,显然是因为对熔金的理论研究还比较简单。在 T. Groenewald 的报告中也提到,虽然 Fe3+ 的存在对金的初始溶解速率很大,但它可以形成稳定的 [Fe2(SO4)3·SCN2H4)]+ 络离子,导致过量随着时间的延长,黄金的溶解率急剧下降。而他在南非对金矿石进行实验时发现,矿浆中可以释放出大量氧化剂,其量足以氧化溶解矿石中三分之二的黄金。他认为:这是矿石中某些物质在参与反应时产生的氧化剂,不需要在浸出液中加入Fe3+。这些氧化剂可能被氧化形成2Au+(SCN2H3)2+2SCN2H4+2H+ 2Au(SCN2H4)2+图1不同Fe3+浓度(g∕L)对金溶解速率的影响) 长春金研究所对小桥金精矿(含S38%)、月儿崖金精矿(含S28%)、四道淘金精矿(含S29%)的铁浸实验证明,在没有其他添加氧化剂的情况下,金的浸出率大于96%,刺入矿浆的铁板上金的沉降回收率≥99.48%。
他们的实验还表明,如果采用上述方法处理具有适当氧化程度的低硫金精矿,则需要增加氧化剂。实验在室温下在搅拌条件下进行。不加氧化剂时,金的浸出率较低;增加H2O20.22~0.31mol,浸出时间4~16h,金的浸出率提高<@1.32~0.6@>27倍(见表2),从表中可以看出,4h浸出时间金的浸出率和改善倍数最大,说明浸出金的初始溶出率很大,而且增加实验者还认为,加入适量的H2O2可使主氧化生成二硫代甲脒:2SCN2H4(SCN2H3)2+2H++2e,提高氧化浸出率。金。但H2O2的氧化能力太强(见表3)2+2H++2e)。@2),增加过多会导致金的强烈氧化和损失,金的浸出会表 2 低硫氧化金精矿中含或不含氧化剂的金浸出率与氧化剂浓度增加∕mol·le比较酸痛时间∕h金浸出率∕%浸出率提高次数∕无H2O2加H2O2H2O2次0.22420.7@>5865.060.6@>27H2O20.3184< @3.757<@1.00<@1.62H2O20.311657.5076.25<@1.32
声明:文章仅代表原作者观点,不代表本站立场;如有侵权、违规,可直接反馈本站,我们将会作修改或删除处理。
图文推荐

2022-05-02 13:58:04

2022-05-02 12:58:05
2022-05-02 11:58:03
2022-05-02 11:05:08

2022-05-02 10:58:03

2022-05-02 10:00:38
热点排行
精彩文章

2022-05-02 14:00:27
2022-05-02 13:58:07

2022-05-02 13:03:03

2022-05-02 13:01:33

2022-05-02 12:58:11

2022-05-02 11:58:05
热门推荐
