
时间:2022-03-25 11:58:04来源:
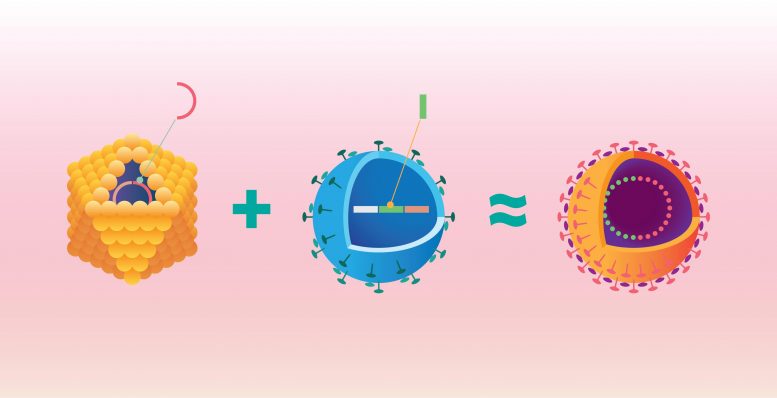
交叉病毒是包含RNA和DNA基因组物质的杂合形式。在这里,包含Rep蛋白序列(指导病毒复制)的单链DNA病毒(黄色)借鉴了RNA病毒(蓝色)的遗传信息,特别是RNA病毒衣壳蛋白的编码序列。结果是同时具有DNA和RNA成分的嵌合病毒–十字花科病毒(见右图)。
数百万年来,病毒参与了广泛的进出口业务,与病毒和非病毒剂交换自身片段并获得新功能。这些微小的实体缺乏外在的复杂性,它们以惊人的能力来弥补模块基因组组件的交换能力,并不断地自我改造。
在发表在《生物》杂志上的新研究中,Arvind Varsani及其同事研究了最近发现的一类病毒,这些病毒已将病毒世界的独特多功能性推向了新的高度。
这些微小的形式被称为十字花科病毒,揭示了RNA和DNA病毒的成分融合,证明了这些先前截然不同的基因组结构域可以在适当的条件下相互混合,从而产生杂种或嵌合病毒变体。
亚利桑那州立大学基础和应用微生物组学生物设计中心的病毒学家Varsani对这些新病毒深感兴趣,这些新病毒开始在更广泛的环境中大量繁殖。
ASU大学副教授Varsani表示:“很高兴看到研究小组在同一时间首次鉴定出十字花科病毒,共同合作共享和挖掘宏基因组学数据,旨在鉴定更大的十字花叶病毒。”生命科学。
Varsani的同事,合著者Kenneth M. Stedman和他在波特兰州立大学的研究小组确定了十字花科病毒的序列。该小组检测到了在极端环境中繁殖的病毒-位于加利福尼亚州北部拉森火山国家公园的沸腾泉湖(BSL)。大约在同一时间,Varsani和Mya Breitbart的研究小组在佛罗里达的蜻蜓样本中鉴定出了一种十字病毒。

Arvind Varsani是基本和应用微生物学生物设计中心和ASU生命科学学院的病毒学家。
自2012年被发现以来,从纽约州北部和佛罗里达州北部的湖泊到南极和深海沉积物中,在全世界的自然环境中都发现了十字病毒。在本研究之前,已鉴定出约80种独特的十字花科病毒,其数量已扩大到461种。
使用称为病毒宏基因组学的技术鉴定了第一批交叉病毒,其中对直接从环境中获得的病毒遗传物质进行测序,而不是从宿主物种或天然水库中进行培养或培养。
这些早期研究的结果揭示了独特的遗传序列,与之前所见的根本不同。这些序列清楚地显示了DNA病毒的特征,但还包含一个似乎源自RNA病毒的基因。
病毒宏基因组学使用a弹枪方法在潜在的巨大序列空间中拖网,使研究人员能够识别环境样本中存在的所有基因组模式,然后分离出不同的病毒序列,就像渔夫从其网中检索各种海洋生物一样。
该技术彻底改变了病毒学的学科。除了鉴定出先前未知病毒的星系之外,宏基因组学还提供了有关遗传稳定性的令人振奋的线索,并正在帮助释放病毒进化的某些秘密,而无需在实验室中最初分离病毒物种或培养病毒。
十字花科病毒属于一类广泛的病毒,称为CRESS(用于环状Rep编码的单链DNA)DNA病毒,最近被分类为Cressdnaviricota门。此类病毒的主要特征是其复制方式,该方式依赖于称为Rep蛋白的特定成分。Rep蛋白对于指导这些病毒的复制方法(称为滚环DNA复制)很重要。Rep蛋白的存在和滚环复制可将一种病毒确定为属于水c病毒,并有助于研究人员解开在病毒世界中发现的极其复杂的关系和血统。
除了在水ress病毒中发现的Rep之外,交叉病毒还具有另一个重要的重要特征-衣壳蛋白,类似于以前仅在RNA病毒中发现的衣壳蛋白。衣壳至关重要,它形成包围病毒身份(其基因序列)的外壳或包膜。衣壳遮蔽了被宿主细胞酶消化而隔离的重要核酸,使病毒颗粒能够将其自身附着于宿主细胞,并允许病毒逃避宿主细胞的防御。最后,衣壳具有特殊的功能,使病毒能够穿透宿主细胞膜并将病毒核酸注入细胞的细胞质。
分析表明,杯状病毒的衣壳蛋白与另一种病毒Tombusviridae的衣壳蛋白密切相关,该病毒是一种已知会感染植物的单链RNA病毒。这种混合病毒特征既包含DNA病毒,又包含RNA病毒衍生的编码成分,这正是使十字形病毒如此独特的原因。
但是,普通的水ress病毒是如何获得其RNA病毒衣壳蛋白编码序列的呢?尽管大概发生了某种形式的横向基因转移,但这仍然是一个颇有争议的问题。
病毒可以从其直接祖先获得基因,这是遗传特征从人类父母传给其后代的方式。但是,病毒在遗传上更加混杂,从它们感染的细胞,其他无关病毒甚至细菌共生体中收集新基因。(这种现象在细菌中也很普遍,可以利用水平基因转移获得抗生素抗性。)
通过某种这样的机制,水ress病毒获得了RNA病毒衣壳样基因,从而产生了第一个十字病毒。似乎各种十字形病毒之间也已经积极地交换了功能元件,从而进一步扰乱了它们的进化历史。
虽然十字形病毒DNA-RNA重组的操作方式仍然是个谜,但WHY可能更直接。显然,从如此遥远相关的病毒源中借用遗传特性的能力可以为单链DNA病毒提供相当大的适应性优势。
在当前的研究中,研究人员探索了一个庞大的数据集,包括从各种环境和生物体中识别出的461种十字花科病毒和10种编码衣壳的环状遗传元件,这使该研究成为迄今为止对十字花科病毒序列进行的最广泛的研究。
在从温带湖泊到多年冻土以及潜伏在包括红藻和无脊椎动物在内的生物体内的环境中发现了这些样品。这项研究指出,伞形藻/藻类/根瘤菌或SAR超群(真核生物的一种自然组合,包括许多光合生物)是这些不寻常病毒的合理候选宿主,尽管这尚未得到证实。
在检查了序列的意外收获之后,研究人员组装了十字病毒蛋白与相关病毒的相似性网络,以试图更好地了解可能引起它们的扭曲进化路径,从而发现许多大病毒家族之间病毒特性的丰富的异花授粉。包括双子病毒科,圆环病毒科,纳米病毒科,Alphasatellitidae,Genomoviridae,Bacilladnaviridae,Smacoviridae和Redondoviridae。
这些发现可能为从RNA作为生命的主要遗传分子到采用更复杂的DNA基因组的早期转变提供新的见解,而DNA已经成为控制细胞世界生命的主要因素。交叉病毒的存在和行为表明,病毒可能在这一至关重要的转变中起着至关重要的作用,在生命的最早出现期间,它充当了RNA和DNA世界之间的一种基因组桥梁,尽管还需要做更多的工作。探索这些可能性。
病毒以无穷无尽的形式重组,已成为地球上最普遍存在的生物实体,影响着每个活生物体并占据着每个生态位。病毒越来越多地自我展示,不仅成为疾病的诱因,而且还成为物种进化的驱动力和生态系统塑造中的重要角色。
交叉病毒从病毒序列空间最远区域借用基因组元件的扩展能力表明,尽管远距离相关形式之间发生大量重组事件,但可能会出现全新的病毒组。
参考:Ignacio de la Higuera,George W. Kasun,Ellis L. Torrance,Alyssa A. Pratt,Amberlee Maluenda,Jonathan Colombet,Maxime Bisseux,Viviane Ravet,Anisha Dayaram,黛西·斯坦顿,西蒙娜·克拉伯格,Peyman Zawar-Reza,Sharyn Goldstien,James V.Briskie,Robyn White,Helen Taylor,Christopher Gomez,David G.Ainley,Jon S.Harding,Rafaela S.Fontenele,Joshua Schreck,Simone G.Ribeiro,Stephen A.Oswald ,詹妮弗·阿诺德(Jennifer M.Arnold),弗朗索瓦·埃诺(FrançoisEnault),阿文·瓦尔萨尼(Arvind Varsani)和肯尼思·M·斯特德曼(Kenneth M.Stedman),2020年9月1日,mBio.DOI:
10.1128 / mBio.01410-20
声明:文章仅代表原作者观点,不代表本站立场;如有侵权、违规,可直接反馈本站,我们将会作修改或删除处理。
图文推荐

2022-03-25 11:58:03

2022-03-25 10:58:04

2022-03-25 09:58:05
2022-03-25 08:58:04

2022-03-24 16:58:03

2022-03-24 16:09:14
热点排行
精彩文章

2022-03-25 10:58:06
2022-03-25 09:58:08

2022-03-25 08:58:07

2022-03-24 10:58:06

2022-03-24 09:58:06

2022-03-24 08:58:05
热门推荐
