
时间:2022-05-02 11:01:36来源:网络整理
主题 2 原子结构和性质
【考试须知】
1、了解元素的第一电离能、电负性等性质的周期性变化,了解元素的电离能与核外电子排列的关系,能够解释元素根据元素电负性在元素周期表中金属和非金属性质的周期性变化。
2、认识元素周期律的本质。掌握同周期同主族元素的原子结构关系和元素性质的梯度规律。了解元素(主族和零族)的原子结构、它们在元素周期表中的位置以及支配其性质发展的规律。
【知识点】
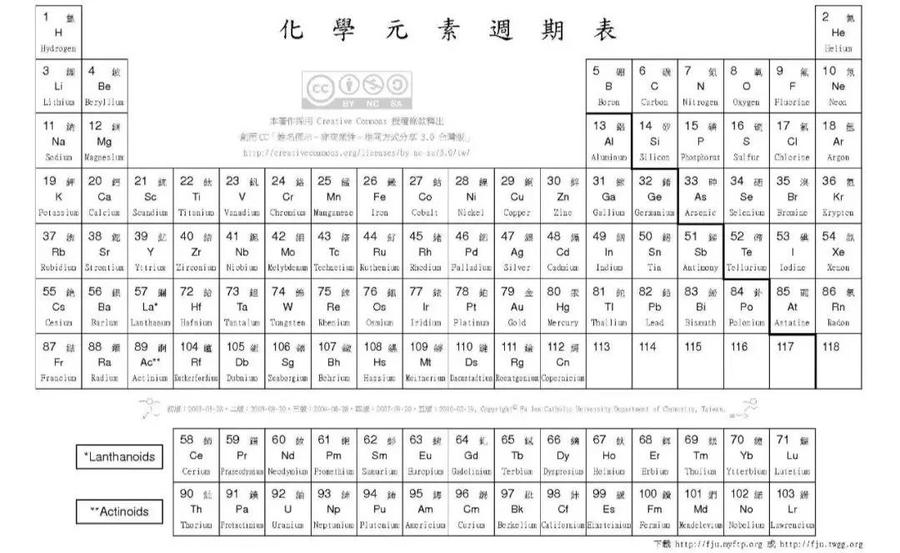
测试点 1:原子结构和元素周期表
1、元素周期表同一行的元素原子含有相同的元素。同一列是一样的。每个循环总是从(ns1)开始,到(ns2np6)结束。这样可以看出元素周期系统的形成是由于排列的周期性重复。
2、随着核电荷数的增加,能级中电子的填充顺序遵循这个原理。不同周期所含元素的种类不一定相同,随着周期数的增加,金属元素的种类逐渐增多,非金属的种类也逐渐增多。
3、元素的分区和族
(1)s区:
,最后一个电子被填满,包括,属于活性金属,分别是碱金属和碱土金属;
(2)p区:
,填入最后一个电子,包括族元素原子结构与元素性质,即非金属和少数金属;
(3)d区:
,最后一个电子被填满,包括族元素,也就是过渡金属;
(4)ds区:
,(n-1)d充满电,最后一个电子被填满,包括,
(5)f区:
,包含元素
区域都是金属元素,非金属元素主要集中。主群主要包含区域,子群主要包含区域,过渡元素主要包含区域。
测试点 2:元素周期律
1、核外电子分布的周期性变化,2、元素主价的周期性变化,
3、金属和非金属,4、原子半径的周期性变化
①电子层数:相同条件下,电子层数越多,半径越大。
②核电荷:相同条件下,核电荷越多,半径越小。
③核外电子数:在核电荷数相同的情况下,核外电子数越多,半径越大。
例子:以下哪个化合物的阳离子半径与阴离子半径之比最小()
A、NaFB、MgI2C、BaI2D、KBr
测试点三:元素电离能和元素电负性
1、电离能变化规律
(1) 分类:
(2)定义:___________________--_______________ 需要转换为 ___________
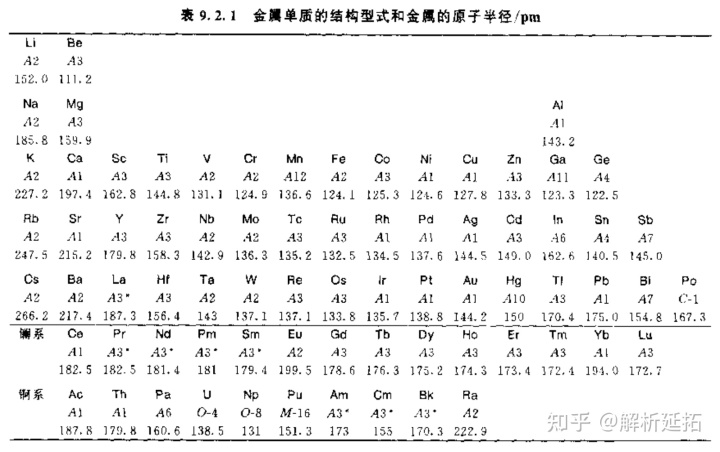
(3)元素第一电离能变化规律
同一个循环:左→右____________________同一个主组:上→下____________________
思考:图中哪些元素的第一电离能异常?为什么?
电力
离开
可以
钠
镁
阿尔
一个
496
738
578
第二
4562
1451
1817
三个
6912
7733
2745
四个
9543
10540
11575
(4)申请:
思考:为什么原子的渐进电离能会增加?这些数据与钠、镁和铝的化合价有何关系?
2、电负性变化规律
(1)提议:
(2)定义:电负性是一个物理量,用来描述不同元素的原子_________________
(3)电负性变化规律
同一时期,主族元素的电负性为_______________原子结构与元素性质,说明_______________增强
在同一主族中,元素的电负性为________,说明其______________逐渐减弱(非金属,氧化性)
元素周期表中电负性最大的元素是______,元素周期表中电负性最小的元素是______
(4)电负性的应用
一个。确定元素类型(一般>1.8、非金属元素;
b.确定化学键的类型(两种元素的电负性差异>1.7、离子键;
c。确定元素的正价或负价(电负性高的为负,电负性小的为正)。
d。电负性是判断金属性和非金属性强弱的重要参数(表征原子获得电子的能力)。
3、对角线法则:左上角和右下角本质上是相似的。如:Li和Mg、Be和Al、B和Si
【在线试题】
1、下列元素组,按原子半径从小到大,按元素第一电离能从大到小依次为
A. K,钠,锂。 N,O,CC。氯,S,PD。铝、镁、钠
2、(2009年安徽)
W、X、Y、Z是元素周期表前36个元素中常见的四种元素,它们的原子序数依次递增。 W和Y的氧化物是引起酸雨的主要物质。 X的基态核外有7个原子轨道,充满电子,Z可以形成红色(或砖红色)Z2O和黑色ZO两种氧化物。
(1)W位于元素周期组的周期表中。W的气态氢化物稳定性比
H2O(g)(填“强”或“弱”)。
(2)Y的基态核外电子排列是Y的第一电离能高于X(填“大”或“小”)。
【教学反思】
声明:文章仅代表原作者观点,不代表本站立场;如有侵权、违规,可直接反馈本站,我们将会作修改或删除处理。
图文推荐

2022-05-02 10:58:03

2022-05-02 10:00:38

2022-05-02 09:58:03

2022-05-02 08:58:03

2022-05-01 19:58:00

2022-05-01 18:58:03
热点排行
精彩文章
![迅捷的TESS捕获了活跃银河系的爆发[视频]](http://www.jjchem.net/uploadfile/2021/0616/2021648122.gif)
2022-05-02 10:58:05

2022-05-02 09:58:06

2022-05-02 08:58:06

2022-05-01 19:58:03
2022-05-01 18:58:05

2022-05-01 17:58:04
热门推荐
