
时间:2021-11-17 15:58:07来源:

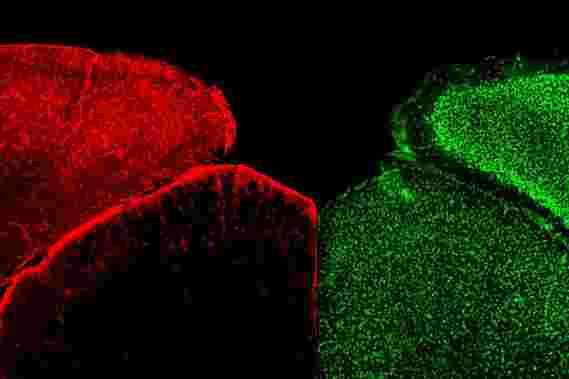
“有很少的特异性或靶向抑制剂用于治疗脑癌。迈克尔·霍曼MIC副教授说,真的有急需新疗法和新想法。该图像的背景显示纳米颗粒(红色)被血液母细胞瘤(以绿色)溶于脑中。核DNA是蓝色的;白色肿瘤相关的巨噬细胞。图像:国家癌症研究所/耶鲁癌中心。
通过切断癌细胞依赖的过程,来自麻省理工学院的研究人员已经确定了停留脑肿瘤的可能的新策略。
麻省理工学院生物学家已经发现了一种基本机制,有助于脑肿瘤被称为胶质细胞瘤积极生长。在封闭小鼠的这种机制后,研究人员能够停止肿瘤生长。
研究人员还确定了一种遗传标记,可用于预测哪种患者最有可能从这种类型的治疗中受益。胶质母细胞瘤通常用辐射和化疗药物替代药物治疗,这可能会延长患者的寿命,但在大多数情况下,不提供治疗方法。
“有很少的特异性或靶向抑制剂用于治疗脑癌。“麻省理工学院综合癌症研究所的麻省理工学院委员会副教授迈克尔Heman(Biit)的副教授Michael Heman说,这是一个急需的恐怖的需求。”
阻断新发现的过程中涉及的关键蛋白质的药物已经存在,至少有一个是在临床试验中治疗癌症。然而,大多数这些抑制剂不会穿过血脑屏障,这将脑与循环血液分离并防止大分子进入大脑。麻省理工学院的团队希望开发能够通过将它们包装成纳米颗粒来越过这级障碍的药物。
在9月28日出现在癌症细胞中的研究是Hemann实验室之间的合作;雅克奎琳李斯,科赫研究所和弗吉尼亚州和D.K.的副主任Ludwig癌症研究教授;和菲利普夏普,一个麻省理工学院学院教授和科赫研究所的成员。本文的引导作者是前麻省理工学院博士线基督教布朗,最近的博士收件人莫妮卡斯卡图,以及研究科学家保罗Boutz。
拼接太多了
几年前,Stanciu和Braun提出了使用一种称为ShRNA的屏幕寻求参与胶质母细胞瘤的基因。该测试涉及使用短链RNA阻断特定基因的表达。使用这种方法,研究人员可以关闭数千个不同的基因,每种肿瘤细胞,然后测量细胞存活的影响。
来自该屏幕的顶部命中之一是蛋白质的基因,称为PRMT5。当该基因关闭时,肿瘤细胞停止生长。以前的研究已经将高水平的PRMT5与癌症联系起来,但蛋白质是可以作用于数百种其他蛋白质的酶,因此科学家不确定如何刺激癌细胞生长。
进一步的实验,其中研究人员分析了当PRMT5被抑制时影响的其他基因导致它们假设PRMT5使用特殊类型的基因剪接以刺激肿瘤生长。需要基因剪接来剪出作为内含子的信使RNA的部分,在将基因复制到mRNA中之后不需要。
2015年,夏普实验室中的其他人发现,大约10%至15%的人mRNA股仍然有一到三个“拘留的内含子”,即使它们是成熟的。由于这些内含子,这些mRNA分子不能离开核。
“我们认为这些股票基本上是MRNA水库。您坐在核中的这些未加工的同种型,让他们被翻译的唯一一件事是一个内涵,“布劳恩说,他现在是Ludwig Maximilian大学慕尼黑大学的医生科学家。
在新的研究中,研究人员发现,PRMT5在调节这种类型的拼接方面发挥着关键作用。他们推测了神经干细胞利用高水平的PRMT5来保证有效的剪接,因此可以表达增殖基因。“随着细胞向其成熟的状态移动,PRMT5水平下降,拘留的内含子水平上升,以及与增殖相关的那些信使RNA在核中被粘在核中,”Lees说。
当脑细胞变成癌性时,通常提高PRMT5水平,并且改善了增殖相关的mRNA的剪接,最终有助于细胞不受控制地生长。
预测成功
当研究人员在肿瘤细胞中阻塞PRMT5时,他们发现细胞停止垂直并进入休眠,非光电状态。PRMT5抑制剂还暂停了植入小鼠皮肤下的胶质母细胞瘤肿瘤的生长,但它们在大脑中的肿瘤中也没有工作,因为交叉血脑屏障困难。
与许多现有的癌症治疗不同,PRMT5抑制剂似乎没有引起重大副作用。研究人员认为这可能是因为成熟细胞不像PRMT5功能上那样依赖于癌细胞。
在纪念Sloan kettering癌症中心的助理成员,奥马尔阿卜杜勒 - ·沃哈卜表示,研究人员以为研究人员曾发现PRMT5是癌症治疗的有希望的潜在目标。学习。
“PRMT5有很多角色,到目前为止,它还没有明确到患有对癌症贡献非常重要的途径,”Abdel-Wahab说。“他们发现的是,其中一个关键贡献是在该RNA剪接机制中,而且,当RNA剪接被破坏时,禁用钥匙途径。”
研究人员还发现了一种生物标志物,可以帮助识别最有可能受益于PRMT5抑制剂的患者。该标记是两种蛋白质的比例,其作为PRMT5的剪接活性的共同因子,并揭示这些肿瘤细胞中的PRMT5是否参与拼接或一些其他细胞功能。
“当您考虑临床试验时,这变得非常重要,因为如果50%或25%的肿瘤会有一些反应,其他人不是,你可能没有办法将其瞄准可能有特定的患者益处。“审判的总体成功可能因对谁对谁能回应而缺乏了解,”Hemann说。
麻省理工学院团队现在正在研究PRMT5在其他类型癌症中的潜在作用,包括肺肿瘤。他们还希望识别他们发现的剪接过程中涉及的其他基因和蛋白质,这也可以制造良好的药物靶标。
研究人员称,该项目由来自几个不同实验室的学生和博士后的学生和邮政编划,提供了一个主要的合作精神和“科学企业家”的典范。
“我认为它真的是一个典型的例子,其中麻省理工学院是一种自下而上的地方,”Lees说。“学生和Postdocs对不同的想法感到兴奋,他们坐在彼此的研讨会上,听到有趣的东西并将它们拉在一起。这真是一个令人惊叹的年轻人在麻省理工学院的创造力的典画。他们无所畏惧。“
该研究由Ludwig Cents的MIT分子肿瘤学院资助,Koch Institue Frentier研究计划通过Kathy和Curt Marble Cander研究基金,国家康复研究所和Koch Institute支持(核心)批准。
出版物:Christian J. Braun等,“致癌成分中的调控内含子的协调剪接在恶性胶质瘤中产生了可利用的脆弱性,”2017年癌症细胞; DOI:10.1016 / J.CCELL.2017.08.018
声明:文章仅代表原作者观点,不代表本站立场;如有侵权、违规,可直接反馈本站,我们将会作修改或删除处理。
图文推荐

2021-11-17 15:58:03

2021-11-17 14:58:02

2021-11-17 13:58:03

2021-11-17 12:58:03
2021-11-17 10:58:02

2021-11-17 09:58:03
热点排行
精彩文章

2021-11-17 15:58:05
2021-11-17 14:58:05

2021-11-17 13:58:05

2021-11-17 12:58:05

2021-11-17 11:58:04

2021-11-17 10:58:04
热门推荐
