
时间:2021-06-30 13:58:02来源:
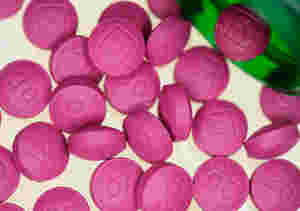
根据美国食品药品监督管理局(USFDA)的一份报告,由于偏离了良好的生产规范,Marksans制药公司的分公司Time-Cap Laboratories Inc.正在从美国市场撤回数量不明的在果阿生产的布洛芬片剂,这是美国市场上的多种优势。
该报告称,由于“投诉与cGMp缺陷有关的气味”,这些片剂/胶囊被召回。它补充说,Marksans药房在其果阿工厂为Time Cap Labs Inc生产了200 mg,400 mg,600 mg和800 mg浓度的片剂以及200 mg浓度的锭剂。
美国食品和药物管理局表示,Time-Cap Laboratories,Inc在全国范围内进行的自愿和正在进行的召回属于II类召回。根据USFDA的规定,II类召回是在“使用或接触违禁产品可能造成暂时或医学上可逆的不良健康后果或极少出现严重不良健康后果的情况下”发起的。
布洛芬是用于治疗疼痛的非甾体类抗炎药。
声明:文章仅代表原作者观点,不代表本站立场;如有侵权、违规,可直接反馈本站,我们将会作修改或删除处理。
图文推荐
2021-06-30 13:58:00

2021-06-30 12:58:00

2021-06-30 12:02:51

2021-06-30 12:02:02
2021-06-30 11:58:00
2021-06-30 10:58:00
热点排行
精彩文章

2021-06-30 13:58:01

2021-06-30 12:58:01

2021-06-30 12:02:16
2021-06-30 11:58:01

2021-06-30 10:58:01

2021-06-30 10:02:13
热门推荐
